COVID Wuhan vs Omicron: Come il Virus Cambia i Nostri Batteri (Studio Rivela Sorprese)
Ciao a tutti! Sono qui per raccontarvi una storia affascinante che ci porta nel cuore della ricerca sul COVID-19, ma da una prospettiva un po’ diversa dal solito: quella dei nostri minuscoli coinquilini, i batteri che formano il nostro microbiota. Ricordate quando è scoppiato tutto? Il SARS-CoV-2 originale, quello di Wuhan, sembrava un nemico implacabile. Poi è arrivata Omicron, super contagiosa ma, per molti, meno cattiva. Ma perché questa differenza? È una domanda che ci siamo posti in tanti, e la risposta potrebbe nascondersi anche nel modo in cui questi virus interagiscono con i batteri che vivono dentro di noi, nei polmoni e nell’intestino.
L’Indagine: Wuhan vs Omicron nel Modello Murino
Per capirci qualcosa di più, abbiamo condotto uno studio comparativo, una sorta di “testa a testa” tra il ceppo originale di Wuhan e la variante Omicron. Ovviamente, non potevamo farlo sugli esseri umani per ragioni etiche e pratiche, quindi abbiamo utilizzato un modello animale molto speciale: topolini transgenici K18-hACE2. Cosa hanno di speciale? Esprimono il recettore umano ACE2, la “porta d’ingresso” che il SARS-CoV-2 usa per infettare le nostre cellule. Questo li rende suscettibili all’infezione in modo simile a noi.
Abbiamo infettato questi topolini con uno dei due ceppi virali (Wuhan o Omicron) attraverso il naso e poi abbiamo osservato attentamente cosa succedeva. Abbiamo monitorato:
- Tassi di mortalità: Quanti topolini sopravvivevano all’infezione?
- Carica virale: Quanto virus c’era nei loro tessuti?
- Danni ai tessuti: Abbiamo analizzato al microscopio i polmoni e la trachea per vedere i segni della battaglia tra virus e ospite.
- Microbiota: E qui viene il bello! Abbiamo analizzato il DNA batterico presente nei polmoni e nelle feci (che riflettono il microbiota intestinale) per vedere come cambiava la composizione di queste comunità microbiche dopo l’infezione.
Risultati Sorprendenti: Due Virus, Due Storie Diverse
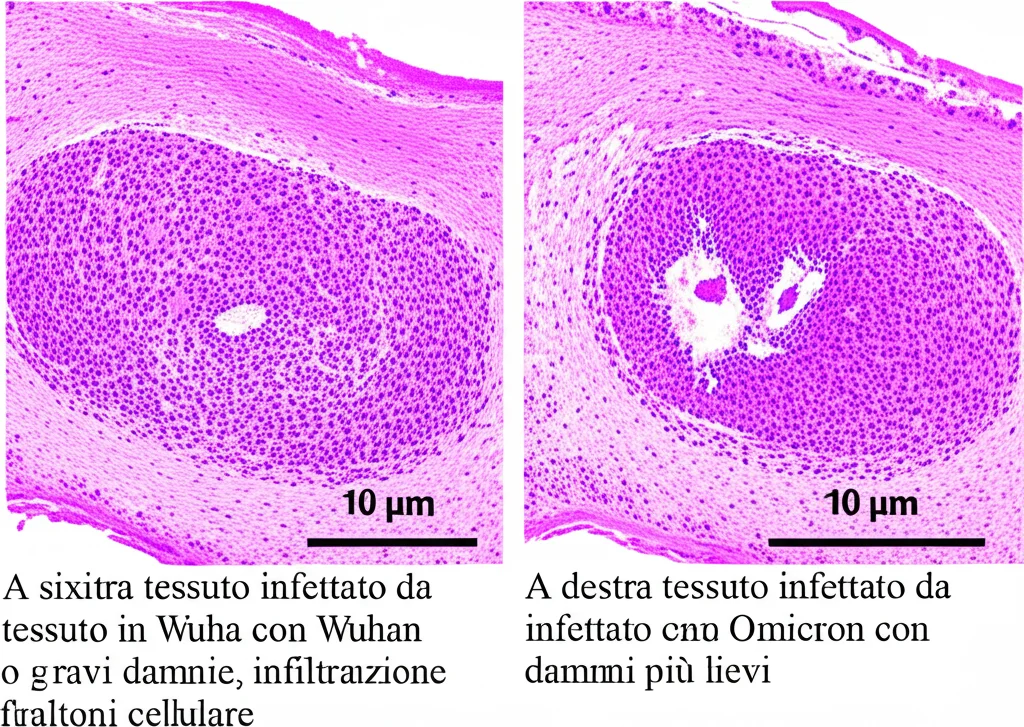
I risultati sono stati netti e, per certi versi, sorprendenti. Come ci si poteva aspettare da quanto visto negli umani, il ceppo Wuhan si è rivelato un vero killer per i nostri topolini: il 100% di mortalità entro circa 6 giorni, con danni gravissimi ai polmoni (ispessimento dei tessuti, emorragie, infiammazione diffusa) e alla trachea (perdita delle ciglia protettive, distacco dell’epitelio).
Omicron, invece, è stata decisamente più ‘gentile’: solo il 10% di mortalità nello stesso periodo. Anche se la carica virale iniziale (a 5 giorni dall’infezione) era simile a quella di Wuhan, diminuiva significativamente dopo 10 giorni. I danni ai polmoni erano più lievi (principalmente un certo ispessimento che persisteva) e anche la trachea mostrava alterazioni meno gravi, sebbene presenti.
Il Microbiota Entra in Scena: Cambiamenti Specifici per Ceppo
Ma la parte forse più intrigante riguarda proprio il microbiota. Qui le cose si fanno complesse e affascinanti. Abbiamo usato tecniche di sequenziamento del gene 16S rRNA (una sorta di “codice a barre” per i batteri) per vedere chi c’era e in che quantità nei polmoni e nell’intestino.
Nei Polmoni:
Analizzando i batteri polmonari, abbiamo notato differenze sottili ma significative. Curiosamente, mentre la diversità generale non cambiava drasticamente, il rapporto tra due grandi gruppi batterici, Firmicutes e Bacteroidetes (il famoso rapporto F/B), aumentava nei topi infetti da Omicron rispetto a quelli infetti da Wuhan. Questo suggerisce un diverso tipo di “scompiglio” microbico.
Andando più nel dettaglio:
- Con Wuhan: abbiamo visto un aumento di batteri legati a Escherichia coli (spesso associato a infezioni opportunistiche) e una diminuzione di altri gruppi come Erysipelotrichaceae (che alcuni studi collegano a risposte immunitarie specifiche, come quelle mediate da IL-4, una citochina spesso elevata nelle infezioni gravi da Wuhan).
- Con Omicron: abbiamo osservato cambiamenti diversi, come una diminuzione iniziale di Bifidobacterium pseudolongum e Kineothrix, e un aumento di alcuni tipi di Eubacterium.
Questi risultati ci dicono che non solo l’infezione altera il microbiota polmonare, ma lo fa in modo diverso a seconda del ceppo virale. L’aumento di E. coli con Wuhan potrebbe essere legato ai danni più gravi alla barriera polmonare, che permettono a batteri normalmente tenuti a bada di proliferare.
Nell’Intestino:
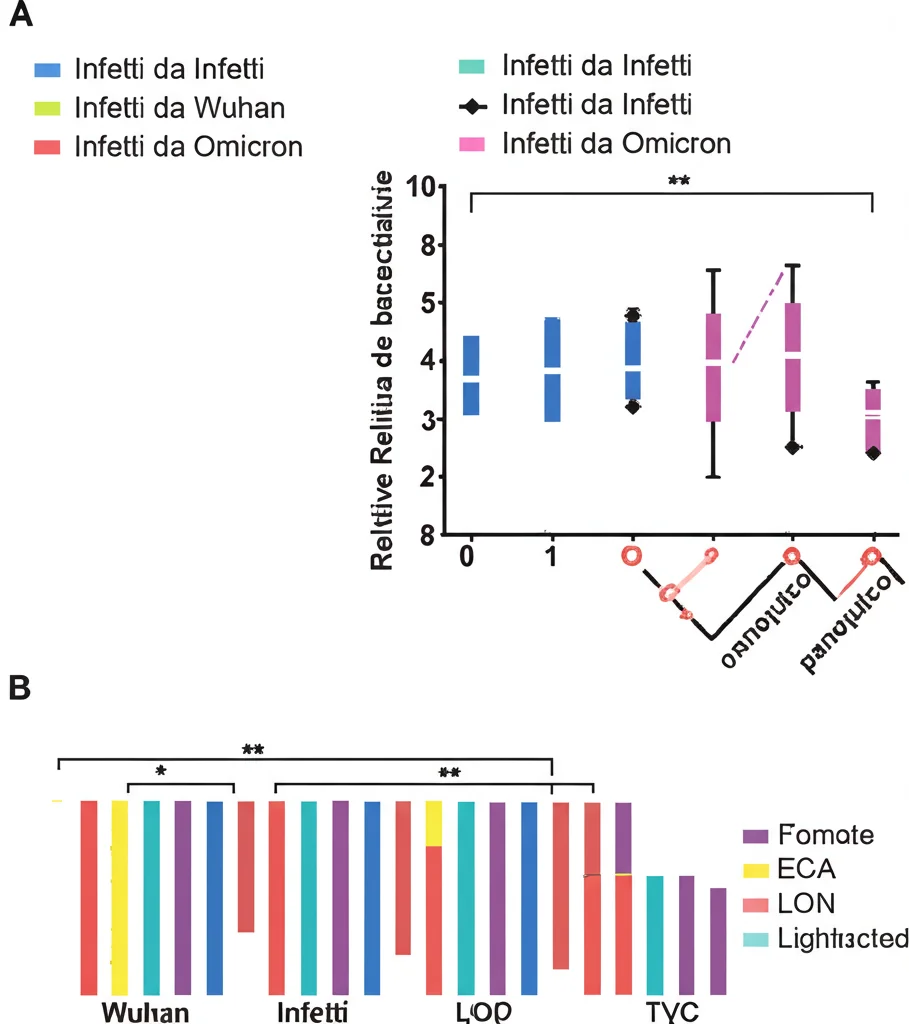
Qui i cambiamenti erano ancora più evidenti! L’analisi statistica (PCoA) mostrava che i gruppi di campioni (non infetti, infetti da Wuhan, infetti da Omicron) si separavano nettamente, indicando alterazioni significative nella composizione del microbiota intestinale.
Cosa abbiamo trovato?
- Sia Wuhan che Omicron hanno causato un aumento di alcuni generi batterici come Oscillibacter, Bacteroides e Pseudoflavonifractor rispetto ai topi sani.
- La diversità delle specie (indice di Shannon) tendeva a diminuire con l’infezione, mentre il rapporto F/B aumentava, soprattutto con Wuhan.
- Una differenza chiave: l’infezione da Wuhan ha portato a un aumento significativo di un batterio chiamato Mucispirillum schaedleri. Questo batterio è interessante: a volte è protettivo, ma in altri contesti è stato associato a infiammazione intestinale (colite) in modelli animali. Questo potrebbe suggerire che Wuhan induca più infiammazione anche a livello intestinale.
- Con Omicron, l’aumento di M. schaedleri non era così marcato inizialmente (a 5 giorni), ma diventava più evidente più tardi (a 10 giorni).
Omicron nel Tempo: Un’Evoluzione Continua
Poiché i topi infetti da Omicron sopravvivevano più a lungo, abbiamo potuto seguire l’evoluzione del loro microbiota tra il giorno 5 e il giorno 10 post-infezione.
Nei Polmoni (Omicron, 5 vs 10 giorni):
Alcuni cambiamenti iniziali (come l’alterazione di B. pseudolongum e Eubacterium_g8) tendevano a tornare verso la normalità al giorno 10. Tuttavia, altri cambiamenti emergevano o si accentuavano:
- Aumento significativo di Faecalibaculum rodentium al giorno 10. Questo batterio (e il suo parente umano Holdemanella biformis) è stato associato alla protezione contro la colite e i tumori intestinali, ma il suo ruolo nei polmoni è tutto da scoprire.
- Diminuzione di diverse specie di Lactobacillus al giorno 10. I lattobacilli sono spesso considerati “buoni”, e alcuni studi suggeriscono che possano proteggere da infezioni respiratorie. La loro diminuzione potrebbe non essere un buon segno a lungo termine.
Questo ci dice che l’infezione da Omicron, pur essendo meno letale, innesca modifiche nel microbiota polmonare che continuano a evolversi nel tempo.
Nell’Intestino (Omicron, 5 vs 10 giorni):
I cambiamenti principali osservati al giorno 5 (aumento di Oscillibacter, Pseudoflavonifractor, Bacteroides, e alterazioni della diversità e del rapporto F/B) persistevano anche al giorno 10. In più, come accennato, l’abbondanza di Mucispirillum schaedleri aumentava significativamente proprio al giorno 10. Questo batterio, insieme all’aumento persistente di Bacteroides vulgatus (trovato elevato in alcuni pazienti con Long COVID), potrebbe suggerire che anche Omicron, sebbene più ‘mite’ all’inizio, possa contribuire a uno stato infiammatorio intestinale o a squilibri che si manifestano più tardi.
Cosa Significa Tutto Questo? Il Microbiota come Attore Chiave
Insomma, questa ricerca ci mostra chiaramente che i diversi ceppi di SARS-CoV-2 non sono tutti uguali, non solo per la gravità della malattia che causano direttamente, ma anche per come “dialogano” e alterano le comunità batteriche nei nostri polmoni e nel nostro intestino.
Abbiamo scoperto alterazioni specifiche del microbiota associate a ciascun ceppo:
- Wuhan sembra indurre cambiamenti più legati a danni tissutali acuti e potenziale infiammazione (E. coli nei polmoni, M. schaedleri nell’intestino).
- Omicron, pur essendo meno aggressiva, provoca comunque uno scompiglio microbico (dysbiosis) sia nei polmoni che nell’intestino, con cambiamenti che evolvono nel tempo e che potrebbero avere implicazioni a lungo termine (pensiamo al Long COVID e al possibile ruolo del microbiota intestinale).
Questi risultati sono importanti perché rafforzano l’idea che il microbiota non sia un semplice spettatore passivo durante le infezioni virali, ma un attore che può influenzare l’andamento della malattia e la risposta del nostro corpo. Le differenze osservate tra Wuhan e Omicron potrebbero in parte spiegare le diverse manifestazioni cliniche e la diversa gravità associate a questi ceppi.
Naturalmente, questo è uno studio su modelli animali e servono ulteriori ricerche per confermare questi meccanismi negli esseri umani e per capire appieno le conseguenze di queste alterazioni microbiche. Ma la strada è aperta: comprendere queste interazioni virus-microbiota potrebbe portare, in futuro, a sviluppare nuove strategie terapeutiche, magari basate proprio sulla modulazione del microbiota (con probiotici, prebiotici, o trapianti fecali mirati) per aiutarci a combattere meglio non solo il COVID-19, ma anche altre infezioni virali. È un campo di ricerca in pieno fermento, e sono sicuro che ne sentiremo parlare ancora molto!
Fonte: Springer