Il Colesterolo ‘Nascosto’: Svelato il Mistero della Resistenza ai Farmaci nel Prolattinoma?
Ciao a tutti! Oggi voglio parlarvi di una scoperta che mi ha davvero affascinato e che potrebbe cambiare il modo in cui guardiamo a un problema medico piuttosto comune: la resistenza ai farmaci nel trattamento del prolattinoma. Avete presente quando una cura, che sulla carta dovrebbe funzionare alla grande, in alcuni pazienti semplicemente non fa effetto come dovrebbe? Ecco, è una situazione frustrante sia per i medici che per i pazienti, e nel caso del prolattinoma, un tumore (fortunatamente spesso benigno) dell’ipofisi, questo accade più spesso di quanto vorremmo.
Il Prolattinoma e la Sfida della Resistenza
Il prolattinoma è il tipo più diffuso di tumore neuroendocrino ipofisario. Produce un eccesso di ormone prolattina, causando una serie di problemi come alterazioni del ciclo mestruale, infertilità, e talvolta anche sindrome metabolica e obesità. La buona notizia è che abbiamo dei farmaci efficaci, gli agonisti della dopamina (come la cabergolina), che agiscono su un recettore specifico chiamato DRD2 (recettore D2 della dopamina). Questi farmaci sono la prima scelta terapeutica e spesso funzionano benissimo.
Però, c’è un “ma”. Circa il 10% dei pazienti, e fino al 20% di quelli con tumori più grandi (macroprolattinomi), sviluppa una resistenza a questi farmaci. Significa che le medicine non riescono a normalizzare i livelli di prolattina o a ridurre significativamente le dimensioni del tumore, anche a dosi standard. Perché succede? I meccanismi esatti sono ancora un po’ un mistero, anche se sappiamo che la presenza del recettore DRD2 sulla superficie delle cellule tumorali è fondamentale.
La Pista Inaspettata: il Colesterolo
Ed è qui che entra in gioco la nostra ricerca. Analizzando il “codice genetico” espresso (il trascrittoma) in campioni di tumore prelevati chirurgicamente, ci siamo imbattuti in qualcosa di inaspettato: un’anomalia nel metabolismo del colesterolo nei prolattinomi, specialmente in quelli resistenti ai farmaci! Questa scoperta ci ha incuriosito parecchio. Già in passato avevamo notato che i pazienti con tumori ipofisari tendevano ad avere il colesterolo alto. Poteva esserci un legame diretto con la resistenza ai farmaci?
Per capirlo meglio, abbiamo fatto degli esperimenti in laboratorio usando una linea cellulare di prolattinoma di ratto (le cellule MMQ). Ebbene sì: aggiungendo colesterolo alle colture cellulari, abbiamo visto che queste diventavano significativamente più resistenti all’effetto della cabergolina. Lo stesso è accaduto in esperimenti su animali (topi con xenotrapianti del tumore): una dieta ricca di colesterolo rendeva il tumore meno sensibile al farmaco. Era chiaro: il colesterolo giocava un ruolo attivo nella resistenza. Ma come?
Il Recettore DRD2: Non Scompare, si Nasconde!
La prima ipotesi logica sarebbe stata: forse il colesterolo riduce la quantità totale del recettore DRD2 nelle cellule? Abbiamo controllato, ma sorprendentemente, il livello totale della proteina DRD2 non cambiava. Allora cosa succedeva? La chiave, abbiamo scoperto, non era la quantità, ma la posizione del recettore.
Il recettore DRD2, per funzionare, deve trovarsi sulla membrana esterna della cellula, pronto a legare il farmaco. Quello che abbiamo osservato è stato affascinante: il colesterolo non eliminava il DRD2, ma lo faceva “ritirare” dalla superficie! Ne riduceva la presenza sulla membrana e ne aumentava la quantità all’interno della cellula, nel citoplasma. È come se la “serratura” (il DRD2) venisse spostata dalla porta d’ingresso (la membrana) all’interno della casa (il citoplasma), rendendo impossibile per la “chiave” (il farmaco) aprire la porta. Questo spiegherebbe perché il farmaco diventa meno efficace. Lo abbiamo confermato sia nelle cellule in coltura (MMQ e GH3) sia nei tumori cresciuti nei topi a dieta ipercolesterolemica.
Il Colpevole nel Meccanismo: i Granuli di Stress
Ok, il colesterolo sposta il DRD2 dalla membrana. Ma *come* lo fa? Per investigare questo meccanismo molecolare, abbiamo usato una tecnica chiamata immunoprecipitazione combinata con spettrometria di massa. In pratica, abbiamo “pescato” il DRD2 dalle cellule e visto quali altre proteine gli si legavano, confrontando cellule trattate con colesterolo e cellule di controllo.
Qui è arrivata un’altra sorpresa. Il colesterolo aumentava il legame tra il DRD2 e un gruppo di proteine note per formare delle strutture chiamate granuli di stress (SGs). Gli SGs sono aggregati temporanei di RNA e proteine che le cellule formano in risposta a condizioni di stress (come, a quanto pare, un eccesso di colesterolo!). Tra le proteine che legavano di più il DRD2 c’era la G3BP1, una proteina “cuore” degli SGs.
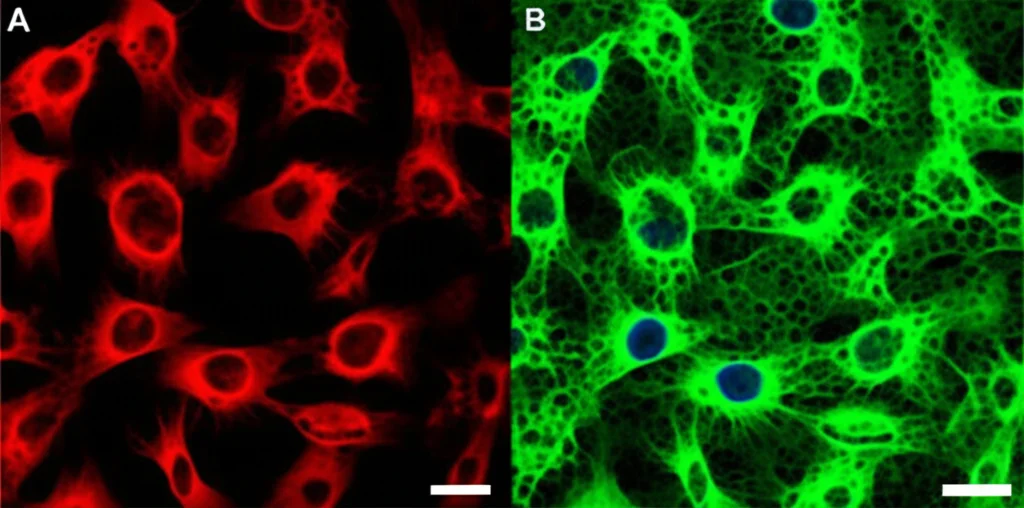
Abbiamo quindi verificato: il trattamento con colesterolo induceva effettivamente la formazione di questi granuli di stress nelle cellule MMQ? La risposta è stata sì. Abbiamo visto un aumento della G3BP1 negli aggregati proteici tipici degli SGs e abbiamo visualizzato gli SGs stessi usando una sonda fluorescente specifica (TASG). Non solo: anche nei tumori dei topi a dieta grassa e, cosa importantissima, nei campioni di prolattinoma umano resistente ai farmaci, abbiamo trovato livelli più alti di G3BP1 rispetto ai tumori sensibili. Il quadro cominciava a delinearsi: Colesterolo -> Formazione di Granuli di Stress -> “Sequestro” del DRD2 lontano dalla membrana -> Resistenza al farmaco.
Bloccare i Granuli di Stress per Ripristinare la Sensibilità
Se la nostra ipotesi era corretta, allora impedire la formazione dei granuli di stress avrebbe dovuto contrastare l’effetto del colesterolo sul DRD2 e sulla resistenza al farmaco. Abbiamo provato due approcci:
- Abbiamo modificato geneticamente le cellule MMQ per far loro produrre più USP10, una proteina che inibisce la formazione degli SGs.
- Abbiamo usato una piccola molecola chiamata ISRIB, nota per sopprimere la formazione degli SGs.
I risultati sono stati entusiasmanti! In entrambi i casi, anche in presenza di colesterolo, la formazione di granuli di stress era ridotta. E cosa più importante: il recettore DRD2 rimaneva localizzato sulla membrana cellulare e le cellule mantenevano la loro sensibilità alla cabergolina! Il colesterolo non riusciva più a indurre resistenza. Questa è stata una conferma cruciale del ruolo centrale degli SGs in questo meccanismo.
Implicazioni Future e Possibili Soluzioni
Questa scoperta apre scenari davvero interessanti. Innanzitutto, suggerisce che gestire i livelli di colesterolo nei pazienti con prolattinoma potrebbe essere ancora più importante di quanto pensassimo, specialmente in quelli che mostrano segni di resistenza ai farmaci.
In secondo luogo, identifica i granuli di stress come un potenziale nuovo bersaglio terapeutico per superare la resistenza. Abbiamo anche fatto un’analisi computazionale (drug repositioning) per cercare farmaci già esistenti che potessero inibire gli SGs e abbiamo identificato l’anisomicina. Esperimenti preliminari in vitro hanno mostrato che anche l’anisomicina può attenuare la resistenza indotta dal colesterolo.
Certo, la strada è ancora lunga. Dobbiamo capire meglio come esattamente gli SGs regolano la posizione del DRD2 e se altri tipi di stress cellulare possono indurre resistenza simile. Ma aver identificato questo legame tra metabolismo del colesterolo, granuli di stress e localizzazione del recettore DRD2 è un passo avanti fondamentale.
In sintesi, sembra che un eccesso di colesterolo possa “stressare” le cellule del prolattinoma, portandole a formare granuli di stress che, a loro volta, “nascondono” il recettore DRD2 dalla superficie cellulare, rendendo i farmaci meno efficaci. Una scoperta che non solo ci aiuta a capire meglio la resistenza nel prolattinoma, ma che potrebbe avere implicazioni anche per altre malattie dove il DRD2 è coinvolto, come il Parkinson. Staremo a vedere cosa ci riserverà il futuro della ricerca!
Fonte: Springer