Cellule LGR5+: Le Super Cattive Nascoste nel Cancro al Polmone Svelate dalla Scienza!
Ciao a tutti, appassionati di scienza e curiosi! Oggi voglio portarvi con me in un viaggio affascinante nel microscopico mondo delle nostre cellule, un mondo dove a volte si nascondono dei veri e propri “super cattivi” che possono mettere a rischio la nostra salute. Parliamo di cancro al polmone, in particolare dell’adenocarcinoma polmonare (LUAD), che purtroppo è il tipo più diffuso e con una mortalità ancora troppo alta. Ma non temete, la ricerca non si ferma mai e oggi vi racconto di una scoperta che potrebbe aprire nuove strade per combatterlo!
Immaginate di avere una lente d’ingrandimento potentissima, capace non solo di vedere le singole cellule, ma di ascoltare cosa dicono, cosa fanno, quali geni accendono e spengono. Ecco, questa è un po’ la magia della sequenza dell’RNA a singola cellula (scRNA-seq), una tecnologia pazzesca che ci sta aiutando a capire meglio i meccanismi più intimi del cancro.
Un’Indagine Hi-Tech nel Cuore del Cancro al Polmone
Recentemente, un team di scienziati (e idealmente, mi ci metto un po’ in mezzo anch’io per come ve la racconto!) ha utilizzato questa tecnica per studiare campioni di tessuto polmonare, sia sani che affetti da LUAD. L’obiettivo? Scovare le caratteristiche delle cellule staminali tumorali (CSCs), quelle cellule un po’ “madri” del tumore, capaci di autorigenerarsi e dare origine a nuove cellule cancerose, rendendo la malattia così difficile da eradicare e incline a recidive e metastasi.
Pensate che analizzando ben 41.322 cellule, i ricercatori sono riusciti a identificarne 9 cluster principali, come se avessero diviso la folla cellulare in gruppi con caratteristiche simili. E indovinate un po’? Le cellule staminali tumorali erano presenti in proporzione maggiore nei campioni di LUAD rispetto a quelli sani. Non solo, ma anche altre cellule come i linfociti T, le cellule mieloidi, le cellule ciliate, i fibroblasti e i mastociti sembravano più abbondanti nel contesto tumorale, suggerendo che tutto il “quartiere” cellulare è coinvolto nella progressione della malattia.
Le Cellule Staminali Tumorali: Registe Occulte della Malattia
Ma cosa rende queste CSCs così speciali e pericolose nel LUAD? Analizzando i geni differenzialmente espressi (cioè quelli più o meno attivi), si è visto che nelle CSCs dei campioni tumorali erano particolarmente “accesi” i percorsi metabolici legati agli aminozuccheri e nucleotidi zuccherini e, cosa cruciale, la via della replicazione del DNA. In pratica, queste cellule sono super equipaggiate per crescere e moltiplicarsi a tutta velocità, come dei motori sempre al massimo dei giri. Geni come MCM3, RNASEH1, RFC2, PRIM2, RFC5, RPA2 (per la replicazione del DNA) e CHIT1, AMDHD2, FPGT, CHIA, NANS, CYB5R1, HEXB, UXS1 (per il metabolismo degli zuccheri) erano significativamente più attivi nei campioni tumorali. È come se avessero una marcia in più per sostenere la loro crescita incontrollata.
Interessante notare che, al contrario, nelle CSCs dei campioni sani erano più attive vie di segnalazione come quella del NF-kappa B e dell’IL-17, che sono spesso coinvolte nelle risposte immunitarie e infiammatorie. Questo ci dice quanto sia diverso il “comportamento” di queste cellule a seconda del contesto.
Ma la storia non finisce qui! I ricercatori hanno voluto scavare ancora più a fondo, suddividendo ulteriormente queste cellule staminali tumorali. E qui è emersa una protagonista particolare: la cellula staminale LGR5+.
Zoom sulle LGR5+: Le Vere Primedonne della Progressione Tumorale
Le CSCs sono state classificate in tre sottotipi principali: le cellule Basali, le cellule di Paneth e, appunto, le cellule staminali LGR5+. E guess what? Le cellule LGR5+ erano decisamente più abbondanti nei campioni tumorali. Questo suggerisce che proprio queste cellule LGR5+ potrebbero essere delle vere e proprie “driver” della progressione del LUAD. Hanno dei geni marcatori specifici, come ARSE e GJB1, che le distinguono.
Per darvi un’idea, le cellule Basali esprimevano marcatori come DSC3, PKP1 e CXCL3, mentre le cellule di Paneth esprimevano CXCL3 e PLCG2. È come se ogni sottotipo avesse la sua “carta d’identità” genetica.
Per confermare l’importanza di questi geni, sono stati fatti esperimenti in laboratorio su linee cellulari: una linea cellulare normale di epitelio polmonare (BEAS-2B) e una di adenocarcinoma polmonare (A549). Ebbene, ad eccezione di DSC3, tutti gli altri geni marcatori dei sottotipi di CSC (ARSE, GJB1, CXCL3, PKP1, PLCG2) erano significativamente più espressi nelle cellule tumorali A549. Una bella conferma!
CXCL3: Un Attore Chiave nel Dramma Cellulare
Parlando di geni specifici, uno che ha attirato l’attenzione è stato CXCL3. La sua espressione proteica era significativamente più alta nelle linee cellulari di LUAD e anche nei campioni di tessuto tumorale umano rispetto al tessuto sano adiacente. Ma cosa fa questo CXCL3? Sembra essere un vero e proprio “facilitatore” per le cellule tumorali.
Silenziando il gene CXCL3 nelle cellule A549, i ricercatori hanno osservato una netta riduzione della loro capacità di migrare (come se avessero le “gambe legate” in un test chiamato wound healing) e di invadere (come se trovassero un muro in un test chiamato trans-well). Non solo: la loro capacità di proliferare (misurata con il test EdU) diminuiva drasticamente, mentre aumentava il loro tasso di apoptosi, cioè di morte cellulare programmata (verificato con la citometria a flusso). Insomma, senza CXCL3, le cellule tumorali sembrano perdere gran parte della loro aggressività. Questo ci dice che CXCL3 gioca un ruolo cruciale nello sviluppo delle cellule cancerose.
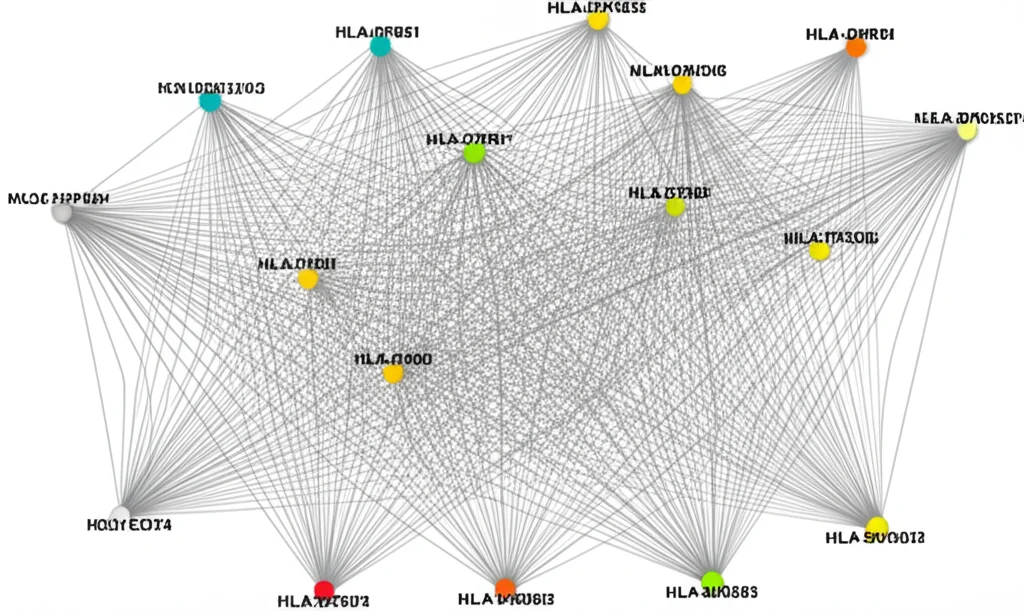
Geni Sotto i Riflettori: Implicazioni per Prognosi e Terapie
Torniamo alle nostre cellule LGR5+. Analizzando i geni differenzialmente espressi in queste cellule, è stata costruita una rete di interazione proteica (PPI). Immaginate una mappa social, ma per le proteine: chi interagisce con chi, chi sono i più “influenti”. Ebbene, sono emersi dei geni “hub”, cioè dei nodi centrali in questa rete, particolarmente importanti per l’attivazione delle cellule staminali tumorali. Tra questi, spiccano nomi come CTSH, HLA-DRB1, HLA-DRA, HLA-DPB1, HLA-DQA1, CD74, HLA-DPA1, HLA-DRB5, HLA-DMA, HLA-C.
La cosa super interessante è che nove di questi dieci geni hub (tutti tranne HLA-C) sono risultati essere fattori protettivi (con un hazard ratio < 1) e significativamente associati alla prognosi dei pazienti con LUAD. Questo significa che la loro espressione potrebbe dare indicazioni su come evolverà la malattia. Inoltre, l'analisi della sensibilità ai farmaci ha mostrato che geni come HLA-DMA, HLA-DQA1, HLA-DRA e CTSH sono correlati significativamente con i valori di IC50 (una misura dell’efficacia di un farmaco) di alcuni farmaci chemioterapici. Questo apre la porta alla possibilità che questi geni possano influenzare la risposta ai trattamenti.
Per esempio, HLA-DPB1 sembra avere un ruolo centrale, essendo regolato da moltissimi microRNA (piccole molecole che controllano l’espressione genica). Altri geni come CD74, CTSH e HLA-DRB5 sono bersaglio di numerosi fattori di trascrizione (proteine che accendono o spengono i geni). Tutto ciò suggerisce che questi geni hub potrebbero essere dei bersagli terapeutici promettenti per colpire le CSC nel LUAD.
Se pensiamo a cosa fanno questi geni:
- HLA-DPB1 codifica per una proteina del Complesso Maggiore di Istocompatibilità di classe II, fondamentale per presentare antigeni extracellulari al sistema immunitario. La sua interazione con altri geni HLA può influenzare l’infiammazione.
- CD74 codifica per una glicoproteina transmembrana, anch’essa legata al MHC di classe II, ed è aumentata in diverse malattie, inclusi i tumori, dove è studiata come bersaglio terapeutico.
- Cathepsin H (CTSH) è stata vista sovraespressa in alcuni tumori e implicata nell’aumento dell’invasività tumorale.
Questi sono solo alcuni esempi, ma ci fanno capire la complessità e l’importanza di queste scoperte.
Reti Complesse e Prospettive Future
Certo, come in ogni studio scientifico, ci sono delle limitazioni. I dati analizzati provengono da database pubblici e sono retrospettivi, quindi serviranno ulteriori studi, magari multicentrici e prospettici, per confermare questi risultati. Inoltre, il meccanismo specifico con cui le cellule LGR5+ promuovono la progressione del LUAD necessita di ulteriori indagini e validazioni su tessuti tumorali.
Tuttavia, questo studio ci ha fornito una mappa incredibilmente dettagliata del panorama cellulare nel LUAD, mettendo in luce il ruolo cruciale delle cellule staminali tumorali, in particolare delle LGR5+. Abbiamo visto come percorsi metabolici specifici e la replicazione del DNA siano fondamentali per il loro mantenimento e come geni hub specifici orchestrino il loro comportamento. L’idea che le cellule LGR5+ possano interagire con le cellule di Paneth per supportare l’autorinnovamento delle CSC, un po’ come avviene nell’intestino, è un’ipotesi affascinante anche per il polmone.
In conclusione, ogni passo avanti nella comprensione di questi meccanismi è una speranza in più. Aver identificato queste cellule LGR5+ e i loro geni chiave potrebbe davvero aprire la strada a nuove strategie terapeutiche più mirate ed efficaci contro l’adenocarcinoma polmonare. E io, da eterno ottimista e appassionato, non vedo l’ora di raccontarvi i prossimi sviluppi!
Fonte: Springer