Occhi Nuovi? Le Cellule del Corpo Ciliare Potrebbero Riparare la Retina!
Ciao a tutti! Oggi voglio parlarvi di qualcosa che mi affascina tantissimo e che potrebbe davvero cambiare le carte in tavola per chi soffre di malattie degenerative della retina, come il glaucoma. Immaginate se potessimo riparare i danni alla vista usando cellule già presenti nel nostro stesso occhio? Sembra fantascienza, ma la ricerca sta facendo passi da gigante!
Il Problema: Neuroni che Non Ricrescono
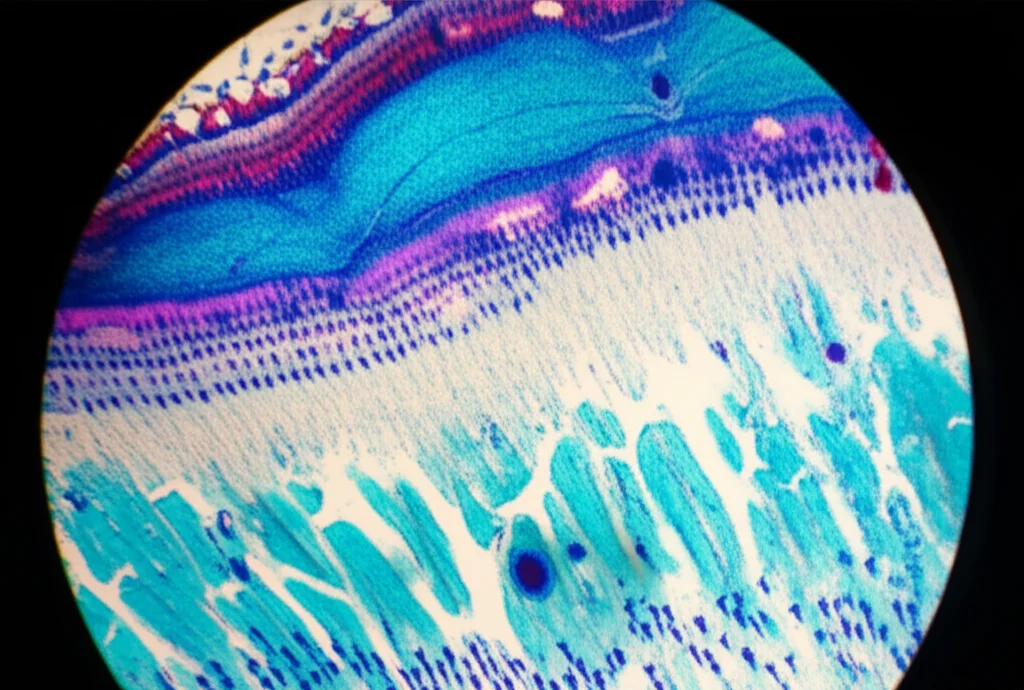
Come sapete, i neuroni del nostro sistema nervoso centrale, una volta danneggiati o morti, tendenzialmente non vengono sostituiti. Questo è un grosso problema nella retina, che fa parte proprio del sistema nervoso centrale. In particolare, due tipi di cellule sono molto vulnerabili: i fotorecettori (quelli che catturano la luce) e le cellule ganglionari retiniche (RGC), che sono come i “messaggeri” finali che inviano le informazioni visive al cervello attraverso il nervo ottico. La perdita di queste cellule è alla base di malattie che portano alla cecità.
Da anni si cercano soluzioni, principalmente attraverso due strade:
- Neuroprotezione: cercare di salvare i neuroni che stanno morendo.
- Sostituzione neuronale: rimpiazzare i neuroni persi con cellule nuove.
Sono state testate tante strategie, incluse terapie cellulari avanzate, ma trovare la fonte ideale di cellule staminali o progenitrici per i trapianti nella retina è ancora una sfida aperta. Si è provato con cellule staminali adulte (MSC) da altre parti del corpo, come il midollo osseo. Queste a volte aiutano a proteggere le RGC, ma spesso non si integrano bene nella retina e possono causare problemi come infiammazione o rigetto.
Una Speranza dall’Occhio Stesso: Il Corpo Ciliare
Qui entra in gioco il protagonista della nostra storia: il corpo ciliare (CB). È una struttura che si trova nella parte periferica dell’occhio. Perché è interessante? Beh, negli animali come pesci e anfibi, una zona simile chiamata “zona marginale ciliare” (CMZ) è una vera e propria fucina di cellule staminali retiniche che possono rigenerare tutti i tipi di neuroni della retina, specialmente dopo un danno! Si pensa che il nostro corpo ciliare sia un po’ il “ricordo evolutivo” di quella zona super-rigenerativa.
E ci sono indizi che anche nei mammiferi il corpo ciliare non sia del tutto “dormiente”. Studi hanno mostrato che in modelli animali di degenerazione retinica, ci sono più cellule progenitrici in proliferazione nel CB. Addirittura, le cellule del CB sembrano avere telomeri più lunghi (le “protezioni” finali dei cromosomi), un segno tipico delle cellule staminali adulte con alto potenziale proliferativo.
Già quasi vent’anni fa, due gruppi di ricerca indipendenti hanno scoperto che cellule isolate dal corpo ciliare di mammiferi adulti potevano, in laboratorio (in vitro), comportarsi come cellule staminali neurali: formavano delle sfere chiamate neurosfere, si moltiplicavano e potevano differenziarsi in nuovi neuroni retinici. Sembrava promettente, no? Però, i tentativi di trapiantare queste cellule nello spazio sotto la retina non avevano dato i risultati sperati.
La Nuova Ricerca: Test sul Campo (anzi, nella Retina!)
Ed eccoci al dunque! Recentemente, un gruppo di ricercatori (di cui idealmente faccio parte in questa narrazione!) si è chiesto: cosa succede se mettiamo queste cellule del corpo ciliare direttamente dentro l’occhio, nel vitreo, in un modello di degenerazione delle RGC? Funzioneranno meglio lì?
Per scoprirlo, abbiamo usato un modello classico: lo schiacciamento del nervo ottico (ONC) nei topi, che causa una morte massiccia e prevedibile delle RGC. Abbiamo isolato cellule dal corpo ciliare (CB) di topi speciali che esprimono una proteina fluorescente verde (GFP), così da poterle seguire dopo il trapianto. Abbiamo usato sia cellule CB “fresche” (primarie) sia cellule amplificate in laboratorio dalle neurosfere (Ns-CB). Per confronto, abbiamo usato anche cellule staminali neurali prese da un’altra area del cervello, la zona subventricolare (Ns-SVZ).
Primo Test: Sicurezza e Comportamento in Retine Sane
Prima di tutto, la sicurezza. Abbiamo iniettato i tre tipi di cellule (CB, Ns-CB, Ns-SVZ) nel vitreo di topi sani. Risultato? Dopo 90 giorni, le cellule erano ancora lì, vive e vegete, formando una sorta di sottile membrana sopra lo strato delle cellule ganglionari, ma senza integrarsi nella retina. Cosa importantissima: non hanno causato danni, né infiammazione (gliosi) né attivazione delle cellule immunitarie della retina (microglia). Questo è già un ottimo punto a favore rispetto ad altre cellule staminali testate in passato!
Secondo Test: Neuroprotezione Subito Dopo il Danno
Poi siamo passati all’azione. Abbiamo indotto il danno al nervo ottico (ONC) e, immediatamente dopo, abbiamo iniettato i nostri tre tipi di cellule. Cosa è successo? In tutti i gruppi trattati, abbiamo osservato un numero significativamente maggiore di RGC sopravvissute rispetto ai topi non trattati, a diversi intervalli di tempo (5, 14 e 45 giorni). Le cellule trapiantate sembravano quindi esercitare un effetto neuroprotettivo, aiutando le RGC danneggiate a resistere più a lungo. Interessante notare che le cellule Ns-CB (quelle espanse in laboratorio) sembravano leggermente più efficaci a lungo termine (45 giorni). Anche qui, le cellule iniettate formavano una membrana senza integrarsi.
Un dettaglio curioso: nelle retine trattate con cellule CB primarie, abbiamo notato che la protezione delle RGC era maggiore proprio nelle zone dove si erano depositate le cellule CB pigmentate (quelle scure). Chissà quale segreto nascondono!

Terzo Test: La Prova del Nove – Possono Sostituire le Cellule Perse?
Ma la domanda cruciale era un’altra: queste cellule possono non solo proteggere, ma anche sostituire le RGC perse? Per verificarlo, abbiamo cambiato strategia. Abbiamo aspettato 45 giorni dopo il danno al nervo ottico, un tempo sufficiente perché la maggior parte delle RGC morisse. Solo allora abbiamo iniettato le cellule CB, Ns-CB e Ns-SVZ. Abbiamo poi analizzato le retine 30 e 90 giorni dopo il trapianto.
E qui la sorpresa più grande! A differenza dei test precedenti, questa volta abbiamo visto che le cellule GFP (soprattutto CB e Ns-CB) non solo formavano la solita membrana, ma alcune di loro si erano integrate nello strato delle cellule ganglionari, proprio dove mancavano le RGC! Ancora più emozionante: analizzando le retine, abbiamo trovato un numero significativamente più alto di cellule che esprimevano marcatori tipici delle RGC (come Brn3a, RBPMS e βIII-tubulina) rispetto ai controlli non trattati.
Nelle retine trattate con CB e Ns-CB, il numero di cellule Brn3a+ era quasi triplicato dopo 90 giorni dal trapianto rispetto ai controlli! Questo suggerisce fortemente che le cellule del corpo ciliare, una volta messe nell’ambiente giusto (una retina “svuotata” delle sue RGC), hanno la capacità di differenziarsi e diventare nuove cellule simili alle RGC.
Anche le cellule Ns-SVZ (quelle del cervello) mostravano una certa capacità di integrazione ed espressione di marcatori RGC, ma sembravano farlo più lentamente rispetto alle cellule CB. Alcune cellule SVZ si sono integrate anche in uno strato più interno (INL) con una morfologia ramificata.
C’è una piccola complicazione tecnica: abbiamo notato, sia in laboratorio che in vivo, che quando le cellule CB si differenziano, tendono a perdere l’espressione della proteina GFP. Quindi, non potevamo vedere direttamente una cellula verde diventare una RGC marcata in rosso, ma l’aumento complessivo dei marcatori RGC in concomitanza con l’integrazione delle cellule trapiantate è un indizio molto forte.

Cosa Significa Tutto Questo?
Questi risultati sono davvero incoraggianti! Ci dicono che le cellule del corpo ciliare, sia quelle fresche che quelle espanse in laboratorio, hanno un potenziale rigenerativo notevole in vivo. A seconda di quando vengono somministrate, possono avere effetti diversi:
- Iniettate subito dopo il danno: Agiscono principalmente come neuroprotettori.
- Iniettate in una retina già danneggiata: Hanno la capacità di integrarsi e differenziarsi, esprimendo marcatori delle cellule perse (RGC).
Inoltre, sembrano essere più “adatte” all’ambiente retinico rispetto alle cellule staminali neurali provenienti dal cervello (SVZ), suggerendo che usare cellule dalla stessa “nicchia” tissutale potrebbe essere vantaggioso. E non dimentichiamo il vantaggio della sicurezza: non hanno causato reazioni avverse significative, a differenza di altre terapie cellulari.
Certo, la strada è ancora lunga. Bisogna confermare che queste nuove cellule siano funzionali, che riescano a riconnettersi correttamente al cervello, e capire come ottimizzare il processo. Sarà anche interessante esplorare se sia possibile stimolare le cellule CB endogene (quelle già presenti nell’occhio) a fare questo lavoro di riparazione senza bisogno di trapianti.
Ma per ora, abbiamo una nuova, promettente pista da seguire. Le cellule del corpo ciliare potrebbero davvero rappresentare una fonte preziosa per future terapie rigenerative per le malattie della retina che ci rubano la vista. È una speranza concreta che ci spinge a continuare a cercare!
Fonte: Springer