CCNE2 e MNAT1: La Coppia Infernale che Rende i Tumori Testa-Collo Resistenti al Cisplatino
Ciao a tutti! Oggi voglio parlarvi di qualcosa che mi appassiona e che, purtroppo, tocca la vita di molte persone: il cancro. Nello specifico, ci tufferemo nel mondo del carcinoma squamoso della testa e del collo (HNSCC), un gruppo di tumori piuttosto eterogenei e, diciamocelo, ostici da trattare.
Uno dei problemi principali che incontriamo nella lotta contro l’HNSCC è la resistenza ai farmaci, in particolare al cisplatino, che è un po’ il pilastro della chemioterapia per queste forme tumorali avanzate. Immaginate la frustrazione: abbiamo un’arma, ma a volte il nemico impara a schivarla, portando a recidive e a prognosi non proprio rosee. Ecco perché c’è un bisogno disperato di capire *come* funziona questa resistenza e, soprattutto, come aggirarla.
Un Indiziato Speciale: La Proteina CCNE2
Nel nostro lavoro di investigazione molecolare, abbiamo messo gli occhi su una proteina chiamata CCNE2 (Ciclina E2). Fa parte della grande famiglia delle cicline, molecole fondamentali che regolano il ciclo di vita delle nostre cellule, un po’ come dei vigili urbani che dirigono il traffico cellulare, specialmente nel passaggio critico dalla fase G1 alla fase S, quando la cellula si prepara a duplicare il suo DNA.
Già sapevamo che CCNE2 non è proprio uno stinco di santo in altri tipi di cancro, dove spesso agisce come un “proto-oncogene”, cioè una di quelle molecole che, se iperattive, possono spingere le cellule verso la trasformazione tumorale. Ma nel contesto dell’HNSCC? Il suo ruolo era ancora avvolto nel mistero.
La nostra ricerca, basata sull’analisi del trascrittoma (l’insieme completo delle molecole di RNA in una cellula) di tessuti HNSCC normali e resistenti al cisplatino (HNSCC/DDP), ha subito fatto suonare un campanello d’allarme: CCNE2 è significativamente più espressa, cioè presente in quantità maggiori, sia nei tessuti tumorali HNSCC che nelle linee cellulari derivate, rispetto ai tessuti sani. E non è finita qui. Analizzando i dati clinici di numerosi pazienti (grazie a database come TCGA e GEO), abbiamo visto una correlazione preoccupante: alti livelli di CCNE2 sono associati a una prognosi peggiore. Insomma, più CCNE2 c’è, meno buone sono le prospettive per il paziente. Abbiamo anche calcolato che CCNE2 ha un buon valore diagnostico (con un’AUC della curva ROC di 0.818), il che significa che potrebbe aiutarci a identificare meglio i pazienti affetti da HNSCC.
Cosa Combina Davvero CCNE2? Tra DNA e Sistema Immunitario
Ok, CCNE2 è alta e questo non va bene. Ma *cosa* fa esattamente per peggiorare le cose? Per capirlo, abbiamo usato tecniche di bioinformatica come l’analisi GO (Gene Ontology) e KEGG (Kyoto Encyclopedia of Genes and Genomes). Queste analisi ci permettono di capire quali processi biologici sono influenzati dai geni correlati a CCNE2. Ebbene, i risultati puntano dritti verso la riparazione del DNA, in particolare la riparazione delle rotture del doppio filamento, e la regolazione del metabolismo del DNA. Questo è super interessante, perché il cisplatino agisce proprio danneggiando il DNA delle cellule tumorali. Se CCNE2 aiuta le cellule a riparare meglio questi danni, ecco spiegata (almeno in parte) la resistenza al farmaco!

Ma CCNE2 sembra avere le mani in pasta anche nel rapporto tra tumore e sistema immunitario. Usando un metodo chiamato ssGSEA, abbiamo esplorato come l’espressione di CCNE2 si lega all’infiltrazione di diverse cellule immunitarie nel tumore. Abbiamo scoperto un quadro complesso:
- Correlazione positiva con cellule T helper, cellule T central memory (Tcm) e cellule Th2.
- Correlazione negativa con cellule dendritiche (DC e pDC) e neutrofili.
Anche l’analisi tramite il database TIMER ha confermato che CCNE2 è legata all’infiltrazione di cellule B, T CD8+, T CD4+ e cellule dendritiche. Questo suggerisce che CCNE2 non solo agisce sulla cellula tumorale stessa, ma modella anche l’ambiente circostante, potenzialmente influenzando la capacità del nostro sistema immunitario di riconoscere e attaccare il cancro.
Spunta un Complice: MNAT1
Continuando a scavare nei dati e analizzando le reti di interazione proteica (PPI), abbiamo identificato un gruppo di geni “hub”, cioè particolarmente importanti e connessi, legati a CCNE2 e alla riparazione del DNA. Tra questi, uno ha attirato la nostra attenzione: MNAT1.
MNAT1 non è un nome nuovo nel mondo del cancro. Fa parte di un complesso chiamato CAK (Cyclin-dependent kinase activating kinase) ed è noto per essere coinvolto nella progressione di altri tumori, come quello al polmone e l’osteosarcoma, influenzando anche lì la sensibilità alla chemioterapia. E nell’HNSCC? Proprio come CCNE2, abbiamo scoperto che MNAT1 è sovraespresso nei tessuti e nelle linee cellulari HNSCC, e anche la sua alta espressione è legata a una prognosi sfavorevole. Il suo valore diagnostico è risultato addirittura leggermente superiore a quello di CCNE2 (AUC = 0.866).
La cosa si fa intrigante: due proteine, entrambe “cattive”, entrambe sovraespresse nello stesso tumore. Sarà un caso? Noi pensiamo di no. Usando modelli computazionali (AlphaFold 3, PRODIGY) abbiamo predetto una possibile interazione fisica diretta tra CCNE2 e MNAT1, con un’energia di legame promettente (-10 kcal/mol). E la conferma è arrivata dal laboratorio: tramite co-immunoprecipitazione (una tecnica che permette di “pescare” una proteina e vedere chi si porta dietro), abbiamo dimostrato che CCNE2 e MNAT1 interagiscono fisicamente nelle cellule HNSCC. L’immunofluorescenza sui tessuti dei pazienti ha poi mostrato che dove c’è tanto CCNE2, c’è anche tanto MNAT1, e viceversa. Sembra proprio che lavorino insieme!

La Prova del Nove: Cosa Succede se Blocchiamo CCNE2? E se Aiutiamo MNAT1?
A questo punto, volevamo vedere gli effetti pratici di questa interazione. Cosa succede se mettiamo i bastoni tra le ruote a CCNE2? Abbiamo usato delle tecniche di silenziamento genico (siRNA) per ridurre l’espressione di CCNE2 nelle cellule HNSCC (CCNE2-KD). I risultati sono stati chiari:
- Le cellule proliferano meno (verificato con saggio EdU).
- Le cellule migrano più lentamente (verificato con saggio “wound healing” o della ferita).
- Le cellule sono meno invasive (verificato con saggio Transwell).
- Abbiamo notato anche cambiamenti nei mitocondri (le centrali energetiche della cellula), che apparivano ridotti in volume dopo il knockdown di CCNE2.
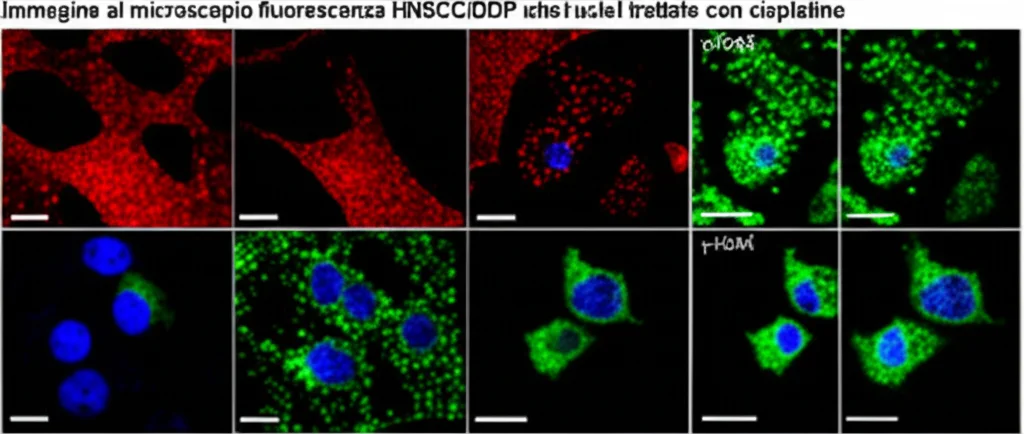
E la resistenza al cisplatino? Abbiamo trattato le cellule HNSCC resistenti (HNSCC/DDP) con cisplatino dopo aver silenziato CCNE2. Usando un marcatore di danno al DNA (γ-H2AX), abbiamo visto che le cellule con meno CCNE2 accumulavano più danni al DNA indotti dal farmaco. Questo significa che silenziare CCNE2 le rende più sensibili alla chemioterapia!
Ora, la domanda cruciale: MNAT1 c’entra davvero? Per verificarlo, abbiamo fatto un esperimento di “salvataggio”: nelle cellule dove avevamo silenziato CCNE2, abbiamo contemporaneamente sovraespresso MNAT1 (MNAT1-OE). E voilà! L’aumento di MNAT1 è stato in grado di annullare in buona parte gli effetti positivi del silenziamento di CCNE2. Le cellule hanno ricominciato a migrare, proliferare e invadere di più, e hanno mostrato meno danni al DNA dopo il trattamento con cisplatino. Questa è una prova forte che CCNE2 esercita i suoi effetti pro-tumorali e pro-resistenza attraverso MNAT1.
Conclusioni: Nuove Armi all’Orizzonte?
Quindi, cosa ci portiamo a casa da tutto questo? Abbiamo scoperto che CCNE2 è un attore importante nella progressione del carcinoma squamoso della testa e del collo e, cosa fondamentale, nella sua resistenza al cisplatino. Non agisce da sola, ma prende di mira MNAT1, formando una sorta di “coppia criminale” che aiuta le cellule tumorali a crescere, diffondersi e, soprattutto, a sopravvivere alla chemioterapia, probabilmente facilitando la riparazione dei danni al DNA indotti dal farmaco.
Questa scoperta è entusiasmante perché apre nuove strade. CCNE2 e MNAT1 potrebbero diventare:
- Biomarcatori prognostici e diagnostici: misurare i loro livelli potrebbe aiutarci a capire meglio l’aggressività del tumore e a identificare i pazienti a rischio.
- Nuovi bersagli terapeutici: sviluppare farmaci che blocchino CCNE2 o la sua interazione con MNAT1 potrebbe essere una strategia per superare la resistenza al cisplatino e migliorare l’efficacia delle terapie attuali.
Certo, la strada è ancora lunga e serviranno ulteriori studi, ma aver identificato questo meccanismo è un passo avanti importante nella comprensione e nella lotta contro l’HNSCC. Speriamo che queste scoperte possano tradursi presto in trattamenti più efficaci per i pazienti.
Fonte: Springer