Pirazoli Verdi e Veloci: La Magia del Mio Nuovo Catalizzatore Magnetico!
Ciao a tutti! Oggi voglio parlarvi di qualcosa che mi appassiona da morire: la chimica verde e come possiamo rendere la sintesi di molecole importanti più efficiente ed ecologica. In particolare, vi racconto del mio ultimo lavoro su un nuovo catalizzatore super performante per creare composti chiamati pirazoli. Sembra complicato? Tranquilli, cercherò di spiegarvelo in modo semplice e, spero, affascinante!
Perché i Pirazoli sono Importanti?
Prima di tutto, perché ci interessano tanto questi pirazoli? Beh, queste molecole sono delle vere star nel mondo farmaceutico. Hanno un sacco di proprietà interessanti: sono antipiretici (abbassano la febbre), analgesici (contro il dolore), anti-infiammatori, antivirali, antidepressivi, anticancro… insomma, un vero tesoro per la nostra salute! Capite bene perché sintetizzarli in modo efficace è fondamentale. Il problema è che i metodi tradizionali spesso richiedono tempi lunghi, basse rese e catalizzatori poco efficienti o difficili da recuperare. Qui entro in gioco io, o meglio, la mia ricerca!
L’Idea: Un Catalizzatore “Intelligente” e Verde
L’obiettivo era chiaro: sviluppare un metodo innovativo, rapido, economico e, soprattutto, rispettoso dell’ambiente per produrre pirazoli. La parola chiave è “catalizzatore”. Un catalizzatore è come un “facilitatore” chimico: accelera una reazione senza consumarsi. Ma volevo qualcosa di più: un catalizzatore che fosse anche facile da recuperare e riutilizzare, in linea con i principi della chimica verde.
La mia idea si è concentrata su un materiale straordinario: l’ossido di grafene (GO). Immaginate fogli sottilissimi, quasi bidimensionali, di atomi di carbonio, con gruppi funzionali contenenti ossigeno sulla superficie. Questo gli conferisce proprietà fantastiche: un’area superficiale enorme (immaginate quanta “piazza” c’è per far avvenire le reazioni!), la possibilità di disperdersi in acqua e, soprattutto, di essere modificato chimicamente.
Ma come renderlo facilmente recuperabile? Semplice: rendendolo magnetico! Ho combinato l’ossido di grafene con nanoparticelle di ossido di ferro (Fe3O4), creando quello che chiamiamo ossido di grafene magnetico (MGO). Ora il nostro materiale di base poteva essere attratto da un magnete, rendendo la separazione dal miscuglio di reazione un gioco da ragazzi! Niente filtrazioni complicate, basta una calamita!
Costruire il Super-Catalizzatore: Passo Dopo Passo
Avere una base magnetica e con grande superficie era ottimo, ma serviva “l’ingrediente segreto” per catalizzare specificamente la sintesi dei pirazoli. Qui la cosa si fa un po’ più tecnica, ma cerco di semplificare.
1. Ancoraggio: Ho prima “agganciato” alla superficie dell’ossido di grafene magnetico una molecola “ponte” chiamata 3-cloropropiltrimetossisilano (PTMS). Questo serve per creare un legame stabile per il passo successivo.
2. Il Ligando Speciale: Ho poi legato a questo ponte una nuova molecola che ho progettato e sintetizzato apposta, un “ligando” chiamato N’1,N’3-bis(2-amminobenzoil)benzene-1,3-disolfonoidrazide (ABDSH). Questo ligando ha la capacità di “afferrare” e tenere fermo l’attore principale della catalisi.
3. Il Cuore Catalitico: Infine, ho immobilizzato su questo complesso lo ioduro di rame (CuI). È il rame, in questa forma, a svolgere il ruolo chiave di catalizzatore, interagendo con le molecole che devono reagire per formare i pirazoli.
Il risultato finale è questo nanocomposito un po’ complesso da nominare: GO@Fe3O4@PTMS@ABDSH@CuI. Ma chiamiamolo semplicemente il nostro “catalizzatore magnetico al rame”.

La Prova del Nove: Sintesi dei Pirazoli
Ok, avevamo il nostro catalizzatore super tecnologico. Era ora di metterlo alla prova! Ho testato la sua efficacia in due tipi di reazioni “one-pot” (cioè, tutti i reagenti messi insieme in un unico passaggio, il che è molto efficiente):
* Reazione a due componenti: Per sintetizzare derivati chiamati 4-(arilmetilene)bis-(3-metil-1-fenil-1H-pirazol-5-olo). In pratica, abbiamo fatto reagire diverse aldeidi aromatiche con la 5-metil-2-fenil-2,4-diidro-3H-pirazol-3-one.
* Reazione a tre componenti: Per creare derivati più complessi, le 3-((fenil)(5-idrossi-3-metil-1-fenil-1H-pirazol-4-il)metil)-4-idrossi-2H-cromen-2-one. Qui abbiamo aggiunto anche la 4-idrossicumarina al mix.
E i risultati? Eccezionali!
Abbiamo ottimizzato le condizioni di reazione (temperatura, quantità di catalizzatore) e scoperto che il modo migliore per farle avvenire era… senza solventi! Questo è un enorme vantaggio per l’ambiente: niente solventi da smaltire!
Le reazioni sono state incredibilmente veloci (parliamo di minuti, tra 4 e 17 minuti a seconda dei reagenti!) e le rese dei prodotti desiderati sono state altissime (tra l’88% e il 95%). Abbiamo anche sintetizzato alcuni derivati di pirazolo completamente nuovi!
Come Funziona la Magia? (Il Meccanismo)
Senza entrare troppo nei dettagli chimici, il cuore del meccanismo sta nel ruolo del CuI nel nostro catalizzatore. Funziona come un “acido di Lewis”: in pratica, attira a sé gli elettroni di uno dei reagenti (l’aldeide), rendendolo più “attivo” e pronto a reagire con le altre molecole (il pirazolone e, nel caso della reazione a tre componenti, la 4-idrossicumarina). Il catalizzatore orchestra l’incontro tra le molecole, facilita la formazione dei nuovi legami e l’eliminazione di una molecola d’acqua, portando alla formazione del pirazolo desiderato. Una volta formato il prodotto, il catalizzatore si “stacca” ed è pronto per un nuovo ciclo.
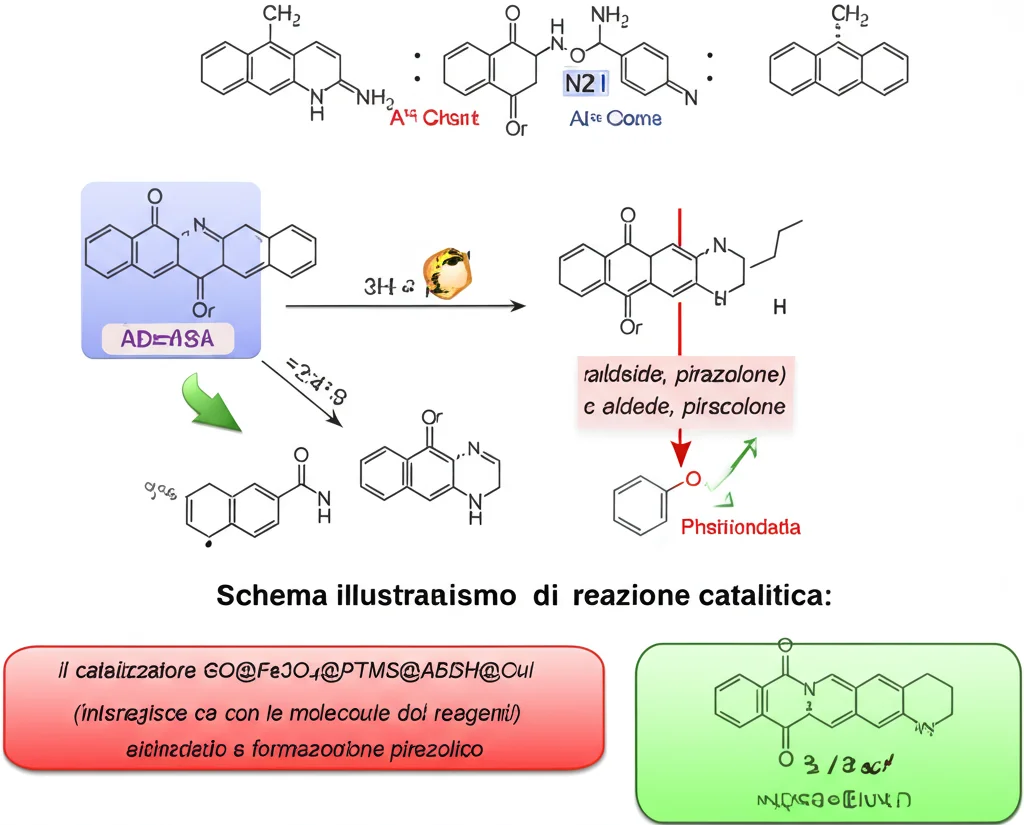
Il Bello della Chimica Verde: Recupero e Riutilizzo
Uno degli aspetti più entusiasmanti è la facilità di recupero e riutilizzo del catalizzatore. Essendo magnetico, alla fine della reazione basta avvicinare una calamita al contenitore: il catalizzatore si attacca al magnete e può essere separato facilmente dal prodotto. Dopo un rapido lavaggio (con un po’ di etanolo caldo) e asciugatura, è pronto per essere riutilizzato!
Abbiamo testato questa capacità di riciclo e abbiamo scoperto che il nostro GO@Fe3O4@PTMS@ABDSH@CuI mantiene un’attività catalitica quasi costante per almeno quattro cicli consecutivi! C’è un leggero calo di efficienza dopo il quarto ciclo, probabilmente dovuto a una minima perdita di rame e ferro durante i lavaggi, ma la stabilità è davvero notevole. Questo non solo rende il processo più economico, ma riduce drasticamente i rifiuti, sposando appieno la filosofia della chimica verde.
Meglio dei Precedenti? Sembra Proprio di Sì!
Abbiamo confrontato le prestazioni del nostro catalizzatore con altri metodi riportati in letteratura per la sintesi di pirazoli simili. I risultati parlano chiaro: il nostro metodo GO@Fe3O4@PTMS@ABDSH@CuI si è dimostrato superiore in termini di:
* Tempi di reazione: Nettamente più brevi (minuti contro decine di minuti o ore).
* Rese: Generalmente più alte.
* Condizioni: Più blande (temperature più basse e assenza di solventi).
* Efficienza del catalizzatore: Ottima attività e facile riciclo.
In Conclusione: Un Piccolo Passo per la Chimica, un Grande Passo per la Sostenibilità
Sono davvero entusiasta dei risultati ottenuti. Siamo riusciti a sviluppare un nanocatalizzatore eterogeneo, magnetico, efficiente e riutilizzabile per la sintesi “one-pot” di importanti derivati pirazolici. Questo approccio non solo semplifica la produzione di queste molecole preziose, ma lo fa in modo molto più sostenibile ed ecologico, grazie alle condizioni senza solventi, ai tempi rapidi, alle alte rese e alla facilità di recupero del catalizzatore.
È la dimostrazione che la ricerca chimica può andare di pari passo con il rispetto per l’ambiente, aprendo la strada a processi industriali più puliti ed efficienti. E chissà quali altre reazioni potremo accelerare con questo piccolo gioiello tecnologico!
Fonte: Springer







