Carcinoma Nasofaringeo: Quando le Cellule Immunitarie Tradiscono e l’EBV Tira le Fila!
Ciao a tutti, appassionati di scienza e misteri del corpo umano! Oggi vi porto nel cuore di una battaglia microscopica, ma dalle conseguenze enormi, che si combatte all’interno di alcuni tumori. Parliamo del carcinoma nasofaringeo (NPC), un tipo di cancro che, come vedremo, ha dei complici subdoli nel nostro stesso sistema immunitario e un “regista” virale ben noto: il virus di Epstein-Barr (EBV).
Cos’è il Carcinoma Nasofaringeo e chi è l’EBV?
Immaginate una forma di cancro che nasce nell’epitelio del rinofaringe, quella parte alta della gola, proprio dietro il naso. Questo è l’NPC. Non è un nemico “democratico”, purtroppo: ha una predilezione geografica ed etnica ben precisa. Pensate che nel 2022, secondo l’OMS, ben l’83,3% dei nuovi casi si è registrato in Asia, con la Cina a fare la parte del leone (circa il 50,9%).
Negli ultimi decenni, la ricerca ci ha insegnato che lo sviluppo dell’NPC è un processo complesso, multifattoriale, dove giocano un ruolo l’ambiente, la genetica e, appunto, l’infezione da virus di Epstein-Barr (EBV).
Esistono diversi tipi istopatologici di NPC, ma nelle regioni ad alta prevalenza come la Cina, oltre il 95% dei casi è di tipo non cheratinizzante ed è fortemente associato all’EBV.
L’EBV è un herpesvirus umano diffusissimo. Spesso l’infezione primaria avviene durante l’infanzia senza dare sintomi, ma se contratta più tardi può causare la famosa mononucleosi infettiva. Dopo l’infezione primaria, l’EBV rimane latente nel nostro corpo per lunghissimo tempo. E qui sta il problema: durante questa latenza, esprime alcuni geni con proprietà pro-oncogeniche. Proteine virali come EBNA1, LMP1, LMP2, e RNA virali come EBERs e BARTs sono stati trovati nelle cellule epiteliali nasofaringee infette. Questi “prodotti” virali contribuiscono all’instabilità genomica e a modifiche del DNA, spingendo le cellule verso la trasformazione maligna. Addirittura, sembra che EBNA1 possa promuovere l’arrivo di particolari cellule immunitarie, le Tregs, attraverso l’aumento di una sostanza chiamata CXCL12.
Le Cellule T Regolatorie (Tregs): Amiche o Nemiche?
Ora, nel nostro sistema immunitario ci sono delle cellule chiamate linfociti T regolatori, o Tregs. Pensatele come dei “pacieri”, il loro compito principale è evitare che il sistema immunitario esageri e attacchi i nostri stessi tessuti sani. Un ruolo nobile, no? Beh, non sempre. All’interno del microambiente tumorale (TME), queste Tregs possono cambiare fazione e aiutare il tumore a sfuggire al controllo immunitario, sopprimendo l’attività antitumorale di altre cellule immunitarie, come i linfociti T CD8+.
In molti tipi di cancro, un’alta infiltrazione di Tregs è associata a una prognosi peggiore. Curiosamente, per l’NPC, alcuni studi passati avevano riportato che una maggiore infiltrazione di Tregs fosse legata a una prognosi migliore. Un bel rompicapo!
Il Problema dei Marcatori e il Nostro Studio
Qui sorge una questione cruciale. Molti di quegli studi si basavano sull’espressione di un singolo marcatore, FOXP3, per identificare le Tregs. Ma affidarsi solo a FOXP3 può essere fuorviante. Perché? Perché FOXP3 può essere espresso anche da altre cellule T attivate che non sono soppressorie, e persino da alcune cellule tumorali! Questo potrebbe portare a un’errata identificazione delle vere Tregs nei tessuti tumorali. Di conseguenza, il ruolo preciso delle Tregs nell’NPC era ancora tutto da chiarire.
Inoltre, la quantità di DNA dell’EBV nel plasma è un indicatore clinico comune della carica virale, ma la sua associazione con il livello di infiltrazione di Tregs nell’NPC non era chiara.
Così, nel nostro studio, abbiamo deciso di andare più a fondo. Abbiamo analizzato i livelli di infiltrazione di Tregs nei tessuti di 103 pazienti con NPC utilizzando una combinazione di marcatori più accettata e specifica: CD4, CD25 e FOXP3 (identificando quindi le cellule CD4+CD25+FOXP3+). Volevamo capire la correlazione tra questa infiltrazione di Tregs “verificate” e i livelli di DNA dell’EBV nel plasma, oltre all’impatto di queste cellule sulla prognosi dell’NPC.
Abbiamo raccolto dati clinici dettagliati e campioni di tessuto per ogni paziente, escludendo chi aveva già ricevuto trattamenti o aveva altri tumori. Per l’analisi del DNA dell’EBV, ci siamo concentrati sui 44 casi più recenti, a causa di un aggiornamento nel metodo di test che ne ha aumentato la sensibilità.
Le analisi sono state fatte usando tecniche di immunofluorescenza multipla e un software apposito (HALO) per analizzare le immagini dell’intero vetrino, garantendo una valutazione completa.
Cosa Abbiamo Scoperto? Le Sorprese non Mancano!
E qui arrivano i risultati, e devo dire che sono piuttosto illuminanti!
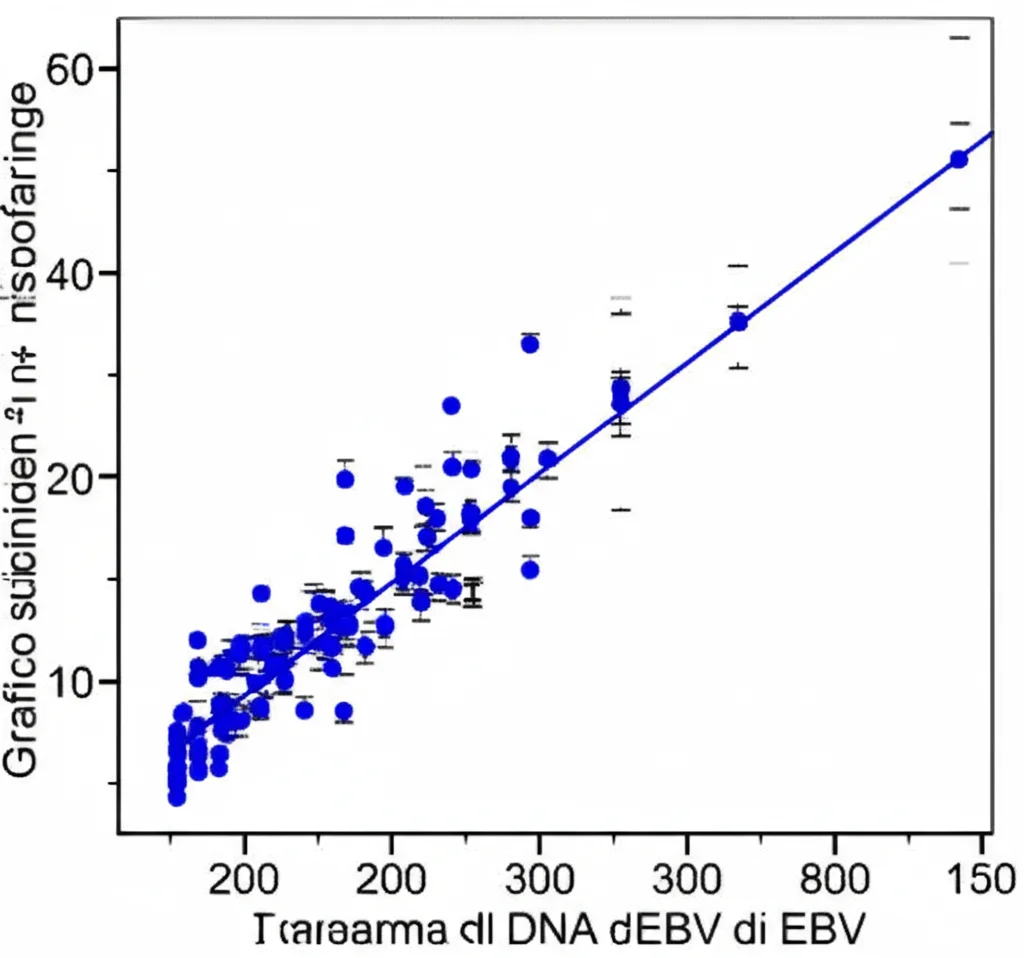
- Abbiamo osservato una correlazione positiva significativa tra l’infiltrazione di Tregs (le nostre CD4+CD25+FOXP3+) nei tessuti tumorali e i livelli di DNA dell’EBV nel plasma (r=0.3428, p=0.02). In parole povere, più DNA virale circolante, più Tregs “nemiche” trovavamo nel tumore.
- Anche l’espressione di CD25 (un componente del recettore per l’interleuchina-2, molto espresso sulle Tregs attive) era positivamente correlata con i livelli di DNA dell’EBV (r=0.3229, p=0.03).
- Passando alla prognosi, abbiamo visto che una maggiore infiltrazione di Tregs era significativamente associata a una peggiore sopravvivenza libera da progressione (PFS) (p=0.03). Non solo, ma questa infiltrazione di Tregs è risultata essere un fattore di rischio indipendente per la progressione dell’NPC (p=0.045). Questo significa che, anche tenendo conto di altri fattori, la presenza massiccia di queste cellule peggiora le cose.
- Un altro dato interessante: un’aumentata infiltrazione di Tregs era negativamente correlata con i linfociti T CD8+ periferici (r=-0.3556, p=0.006). I CD8+ sono i “killer” del sistema immunitario, quelli che dovrebbero eliminare le cellule tumorali. Se le Tregs aumentano e i CD8+ diminuiscono, il quadro non è roseo.
- Infatti, la proporzione di linfociti T CD8+ periferici nei pazienti con NPC in stadio avanzato era significativamente più bassa rispetto a quelli con malattia in stadio iniziale (p=0.02).
Per quanto riguarda la sopravvivenza globale (OS), non abbiamo osservato differenze statisticamente significative, ma questo potrebbe essere dovuto al numero relativamente basso di eventi di decesso nel nostro campione.
Interpretiamo i Dati: Un Puzzle che Prende Forma
Questi risultati ci dicono parecchio. Il DNA dell’EBV nel plasma è un marker tumorale prezioso per l’NPC, riflettendo sia il carico tumorale sia il carico di DNA dell’EBV nel tumore. La correlazione positiva che abbiamo trovato tra DNA dell’EBV plasmatico e Tregs infiltranti suggerisce che alti livelli di DNA dell’EBV sono associati a un microambiente tumorale più immunosoppressivo. Questo è in linea con ricerche precedenti che indicavano come l’EBV potesse espandere le Tregs.
Sembra proprio che l’attività replicativa dell’EBV possa essere un indicatore dello stato immunosoppressivo dell’NPC. Come fa l’EBV? Ad esempio, la sua proteina EBNA1 può stimolare la produzione di TGF-β1 (che promuove la differenziazione delle Tregs) o aumentare chemochine come CCL20 e CXCL12, che facilitano la migrazione delle Tregs verso il tumore. Alti livelli di Tregs, a loro volta, compromettono l’efficacia delle cellule immunitarie effettrici, contribuendo alla progressione del tumore. Questo potrebbe anche spiegare la limitata efficacia di alcuni vaccini mirati contro l’EBV in pazienti con NPC avanzato.
I nostri risultati sulla prognosi differiscono da alcuni studi precedenti, e crediamo che la discrepanza stia proprio nell’uso di marcatori diversi per identificare le Tregs. Come dicevo, basarsi solo su FOXP3 non è abbastanza specifico. Usare il trio CD4+CD25+FOXP3+ offre una maggiore precisione e chiarezza. La nostra ricerca, ancora in corso, indica persino che FOXP3 è espresso anche nelle cellule di NPC positive all’EBV!
La correlazione negativa tra Tregs infiltranti e CD8+ T periferici supporta indirettamente i nostri risultati: se studi precedenti hanno dimostrato che pazienti con NPC con elevati CD8+ T circolanti hanno una sopravvivenza migliore, allora è logico che un’alta infiltrazione di Tregs (che li “combattono”) sia associata a una prognosi peggiore.
Un punto di forza del nostro studio è stato l’analisi dell’intero vetrino, che permette una valutazione più completa dell’infiltrazione di Tregs rispetto alla selezione casuale di alcuni campi visivi.
CD25: Un Attore da Tenere d’Occhio?
CD25, la catena alfa del recettore per l’interleuchina-2 (IL-2), è altamente espresso nelle Tregs. Queste cellule inibiscono la risposta immunitaria legando competitivamente l’IL-2, una citochina essenziale per l’attivazione e la proliferazione di altre cellule immunitarie. In pratica, le Tregs “rubano” l’IL-2, indebolendo la capacità del sistema immunitario di eliminare le cellule dannose.
Un’alta espressione di CD25 nelle Tregs CD4+CD25+FOXP3+ è stata riportata come fattore di rischio indipendente per una prognosi infausta nel cancro del colon-retto. Nel nostro studio, abbiamo valutato il ruolo predittivo di CD25 anche nell’NPC. Sebbene non abbiamo trovato una differenza statisticamente significativa nella PFS tra i gruppi ad alta e bassa espressione di CD25, l’analisi univariata ha suggerito che CD25 influenzasse significativamente la PFS. Questo effetto non è stato confermato nell’analisi multivariata, ma suggerisce che CD25 potrebbe avere un valore predittivo potenziale nell’NPC e merita ulteriori indagini con un campione più ampio.
Conclusioni (Provvisorie) e Prospettive Future
In sintesi, utilizzando marcatori tripli (CD4, CD25, FOXP3), abbiamo identificato le Tregs infiltranti nel tumore come un fattore prognostico negativo indipendente per la progressione dell’NPC. Abbiamo anche trovato che una maggiore infiltrazione di queste Tregs è positivamente associata ai livelli di DNA dell’EBV nel plasma e a una diminuzione dei linfociti T CD8+ periferici.
Certo, il nostro studio ha delle limitazioni, come la dimensione del campione relativamente piccola per alcune analisi, dovuta alla necessità di utilizzare campioni più recenti per garantire la qualità della colorazione. Saranno necessari studi futuri con campioni più ampi per validare ulteriormente questi risultati.
Il prossimo passo? Concentrarci sulla delucidazione dei meccanismi molecolari specifici con cui l’EBV modula l’infiltrazione delle Tregs. Capire questo potrebbe aprire la strada a nuove, più efficaci strategie di immunoterapia per l’NPC. La battaglia è ancora lunga, ma ogni scoperta ci avvicina un po’ di più alla meta!
Fonte: Springer