Cancro Esofageo: Ho Scoperto le Cellule Killer ‘Traditrici’ che Aiutano il Tumore
Ciao a tutti! Oggi voglio parlarvi di un argomento che mi sta molto a cuore e su cui ho lavorato intensamente: il cancro esofageo. Sapete, è una di quelle malattie davvero toste, una delle principali cause di morte per cancro nel mondo. Nonostante i progressi nelle cure, la prognosi spesso rimane infausta. Perché? Beh, in parte a causa di un fenomeno subdolo chiamato immunoevasione: in pratica, il tumore impara a nascondersi e a neutralizzare le difese del nostro sistema immunitario.
Il Campo di Battaglia: il Microambiente Tumorale (TME)
Immaginate il tumore non come una massa isolata, ma come un complesso ecosistema, il Tumor Microenvironment (TME). Qui convivono cellule tumorali, vasi sanguigni, fibroblasti e, crucialmente, cellule immunitarie. Tra queste, le mie “preferite” (scientificamente parlando, ovvio!) sono le cellule Natural Killer (NK). Sono parte della nostra immunità innata, la prima linea di difesa. Il loro compito? Riconoscere e distruggere le cellule tumorali o infette, senza bisogno di un “addestramento” preventivo come altre cellule immunitarie. Fantastiche, vero?
Il Mistero delle Cellule NK nel Cancro Esofageo
Il punto è che nel cancro esofageo, queste cellule NK sembrano non funzionare come dovrebbero. Come mai? Cosa succede nel TME che le rende inefficaci o, peggio, che le “corrompe”? Questa è stata la domanda che mi ha spinto ad approfondire. Volevamo capire meglio gli stati funzionali delle cellule NK in questo specifico tipo di tumore.
Per farlo, ci siamo tuffati nell’analisi di dati complessi: abbiamo integrato dati di RNA-seq (che ci dicono quali geni sono attivi nelle cellule) da grandi database come TCGA e GEO, con dati di single-cell RNA-seq, che ci permettono di guardare l’attività genica cellula per cellula. Un lavoro certosino, ma fondamentale.
La Scoperta: l’NK Score e la Proteina SAMD3
Analizzando questi dati, abbiamo costruito quello che abbiamo chiamato un “NK score”. È una sorta di firma molecolare derivata dai marcatori più importanti espressi dalle cellule NK nel contesto del cancro esofageo. Abbiamo usato tecniche statistiche avanzate (come la regressione LASSO-Cox) per identificare i geni chiave. E qui è arrivata la sorpresa.
Abbiamo scoperto che un NK score elevato era associato a una prognosi peggiore per i pazienti. In altre parole, una certa “configurazione” delle cellule NK nel tumore era un segnale negativo. Ma quale configurazione? Due geni sono emersi come cruciali per questo score: CD7 e, soprattutto, una proteina di cui si sapeva pochissimo in questo contesto, la SAMD3 (Sterile Alpha Motif Domain-containing protein 3).
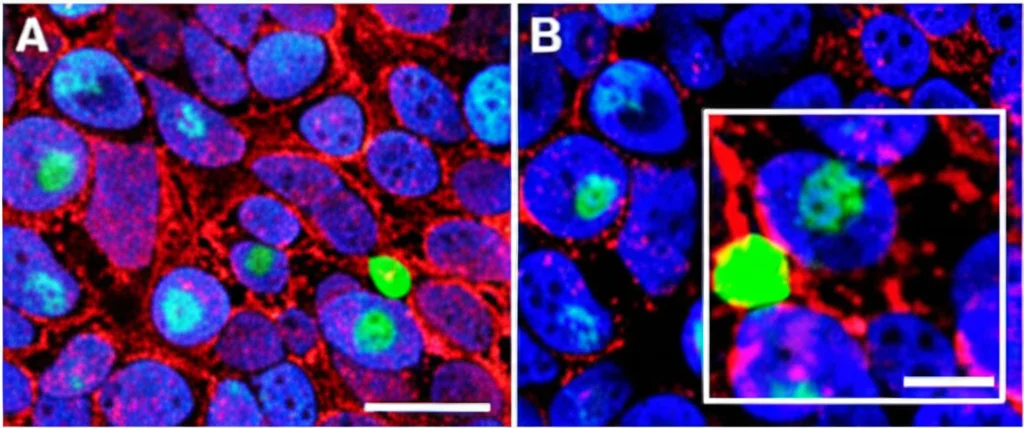
Abbiamo quindi usato tecniche di immunofluorescenza (che colorano specifiche proteine nei tessuti) per andare a vedere direttamente queste cellule nei campioni tumorali dei pazienti. Ebbene sì: abbiamo trovato che le cellule NK presenti nel tumore esprimevano livelli significativi di SAMD3. E, cosa ancora più importante, un’alta densità di queste cellule NK SAMD3+ era correlata a una sopravvivenza più breve e a una risposta peggiore alla chemioterapia adiuvante a base di platino. Sembrava proprio che queste cellule fossero legate a un esito infausto.
SAMD3: Un Freno per le Cellule Killer?
A questo punto, l’ipotesi era chiara: e se SAMD3 agisse come un freno per le cellule NK, riducendo la loro capacità di uccidere le cellule tumorali? Per verificarlo, siamo passati agli esperimenti in laboratorio.
Abbiamo preso una linea cellulare di NK (le NK-92MI) e abbiamo “spento” il gene SAMD3 usando tecniche di ingegneria genetica (shRNA lentivirale). Poi abbiamo messo queste cellule NK “modificate” (con SAMD3 ridotto) a contatto con cellule di cancro esofageo (linee TE-1 e KYSE-30) in una piastra di coltura (in vitro). Il risultato? Le cellule NK senza SAMD3 erano molto più efficaci nell’indurre la morte (apoptosi) delle cellule tumorali rispetto alle cellule NK normali!
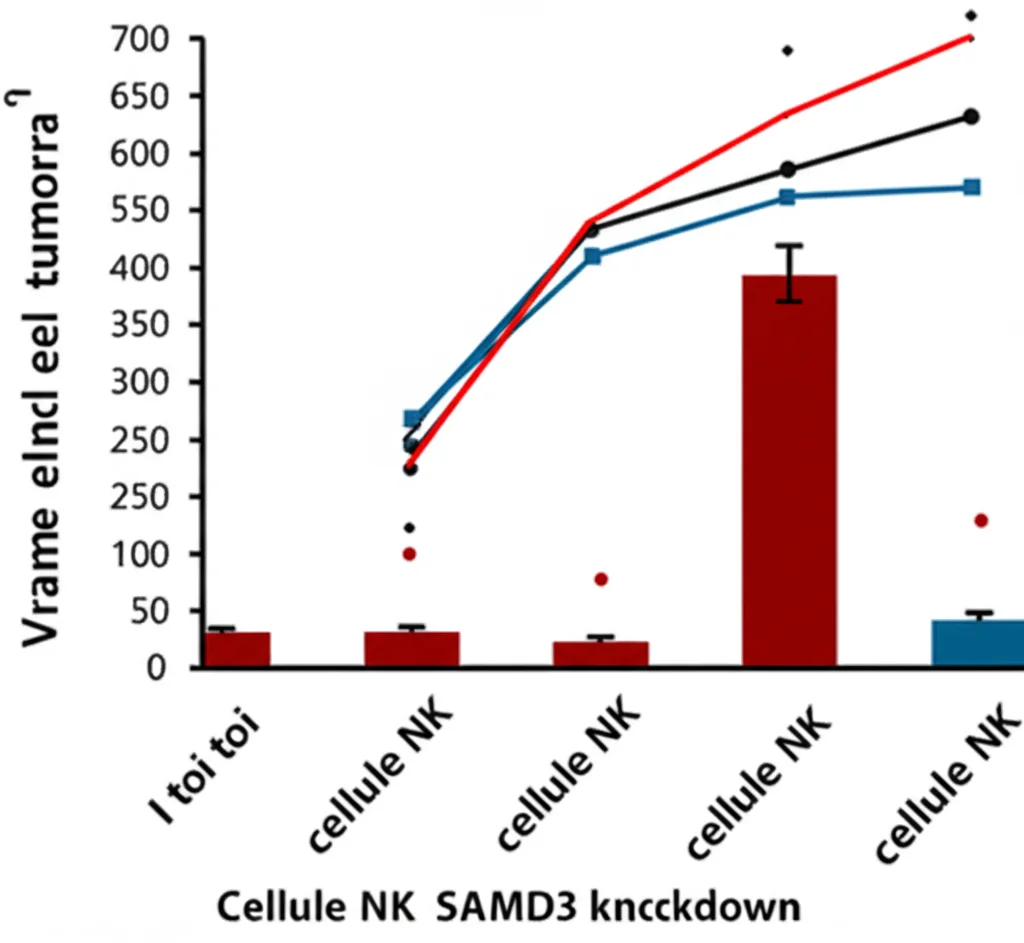
Non contenti, abbiamo fatto un passo ulteriore, usando modelli animali (in vivo). Abbiamo impiantato cellule tumorali esofagee in topi immunodeficienti (modello xenograft). Una volta formato il tumore, abbiamo iniettato in alcuni topi le cellule NK normali e in altri le cellule NK con SAMD3 “spento”. I risultati sono stati netti: nei topi trattati con le cellule NK modificate, la crescita tumorale era significativamente rallentata e i tumori erano più piccoli.
Cosa Significa Tutto Questo? Implicazioni e Prospettive Future
Questi risultati sono, a mio parere, entusiasmanti. Per la prima volta, abbiamo identificato le cellule NK SAMD3+ come potenziali “architetti” dell’immunosoppressione nel microambiente del cancro esofageo. Non sono le solite cellule killer che ci aspettiamo, ma sembrano contribuire a un ambiente che protegge il tumore.
Questo apre nuove strade terapeutiche. Se SAMD3 frena le cellule NK, forse inibire SAMD3 potrebbe “sbloccarle” e potenziare la risposta immunitaria contro il tumore. Potrebbe essere una strategia da sola o, ancora più promettente, in combinazione con le immunoterapie esistenti, come gli inibitori dei checkpoint immunitari (ICI), che spesso non funzionano in tutti i pazienti proprio a causa di questi meccanismi di resistenza. Inibire SAMD3 potrebbe rendere i tumori più sensibili agli ICI.
Ovviamente, come in ogni ricerca seria, ci sono delle limitazioni. Abbiamo lavorato principalmente su dati retrospettivi e modelli preclinici. Serviranno studi prospettici su coorti di pazienti più ampie e trattate in modo uniforme per validare definitivamente l’NK score e il ruolo di SAMD3 come biomarcatore e bersaglio terapeutico. Inoltre, la mancanza di modelli murini immunocompetenti specifici per il cancro esofageo rende difficile studiare tutte le sfumature dell’interazione immunitaria in vivo.
Ma la strada è tracciata. Abbiamo identificato un nuovo potenziale cattivo (SAMD3 sulle cellule NK) e una possibile strategia per combatterlo. La speranza è che questa ricerca contribuisca a sviluppare terapie più efficaci e personalizzate per i pazienti affetti da questa difficile malattia. Il viaggio è appena iniziato, ma ogni passo avanti è una vittoria nella lotta contro il cancro.
Fonte: Springer