Moscerini Insonni? Svelato il Segreto del Glutammato che Ci Fa Dormire!
Ciao a tutti, appassionati di scienza e misteri del sonno! Oggi voglio portarvi con me in un viaggio affascinante nel minuscolo cervello di un moscerino della frutta, la *Drosophila melanogaster*. Sembra incredibile, vero? Eppure, questi piccoli insetti sono dei veri e propri campioni per noi scienziati che cerchiamo di svelare i segreti di comportamenti fondamentali come, appunto, il sonno.
Il Sonno: Un Bisogno Universale (Anche per i Moscerini!)
Il sonno è una di quelle cose che diamo per scontate, ma pensateci: è un comportamento conservato in tutto il regno animale, dai vermi agli esseri umani. È essenziale per la nostra salute, la memoria, l’umore… insomma, per tutto! E la *Drosophila*, con il suo comportamento simile al sonno e un corredo genetico più “maneggevole” del nostro, è diventata un modello preziosissimo per capire come viene regolato. Sappiamo che ci sono meccanismi circadiani (il nostro orologio biologico) e omeostatici (il bisogno di dormire che si accumula stando svegli) che lo controllano, proprio come nei mammiferi.
Il Glutammato: Amico o Nemico del Sonno?
Qui le cose si fanno interessanti. Il glutammato è il principale neurotrasmettitore eccitatorio sia nel nostro cervello che in quello dei moscerini. Nei mammiferi, è generalmente considerato un segnale che ci tiene svegli, attivo. Ma nella *Drosophila*? Beh, gli studi precedenti erano un po’ contraddittori. Alcuni suggerivano che attivare i neuroni che usano glutammato facesse dormire meno i moscerini, altri invece che certi recettori del glutammato fossero necessari per dormire bene. Un bel rompicapo!
Il punto è che l’effetto del glutammato dipende molto da dove agisce e su quale tipo di recettore si lega. Può eccitare direttamente un neurone, oppure può attivare neuroni che a loro volta inibiscono altri circuiti (ad esempio, attivando neuroni GABAergici), o addirittura, come vedremo, può avere un effetto direttamente inibitorio!
La Nostra Indagine: A Caccia del Meccanismo
Nel nostro studio, abbiamo deciso di andare a fondo. Per prima cosa, abbiamo “disturbato” la segnalazione del glutammato in generale, usando tecniche di silenziamento genico (RNAi) per ridurre la proteina che carica il glutammato nelle vescicole sinaptiche (la vGluT). Risultato? I moscerini dormivano significativamente meno durante la notte e il loro sonno era più frammentato, con pisolini più brevi e frequenti. Questo ci ha suggerito che, almeno in parte, il glutammato nella *Drosophila* gioca un ruolo nel promuovere e consolidare il sonno notturno.
Ma quale recettore era il responsabile? Abbiamo passato in rassegna ben 14 diversi tipi di recettori del glutammato conosciuti nel moscerino, silenziandoli uno per uno nei neuroni. E qui la sorpresa: mentre molti non avevano effetti drastici o ne avevano di parziali, il silenziamento di un particolare recettore, chiamato GluClα (un canale del cloruro attivato dal glutammato), ha causato una drastica riduzione del sonno notturno, un aumento degli episodi di sonno e una loro durata più breve. Bingo!

Per essere sicuri, abbiamo anche studiato moscerini mutanti per il gene GluClα. Poiché i mutanti completi non sopravvivevano, abbiamo combinato due diverse mutazioni “deboli” (alleli ipomorfi). Anche questi moscerini “trans-eterozigoti” mostravano una significativa riduzione del sonno notturno e una maggiore frammentazione. Stessa cosa usando una mutazione in combinazione con una delezione che rimuoveva gran parte del gene. Tutte le prove puntavano su GluClα come attore cruciale per un buon sonno notturno.
Dove Agisce GluClα? La Caccia ai Neuroni Giusti
Ok, GluClα è importante. Ma dove nel sistema nervoso deve funzionare per regolare il sonno? Abbiamo usato un arsenale di strumenti genetici (il sistema Gal4/UAS) per silenziare GluClα in diverse aree del cervello e del sistema nervoso. Due linee guida (driver Gal4), la 23E10-GAL4 e la c205-GAL4, hanno dato risultati eclatanti: silenziando GluClα con queste linee, il sonno notturno diminuiva drasticamente. Entrambe queste linee marcano dei neuroni in una struttura cerebrale chiamata “corpo a ventaglio dorsale” (dFB), già nota per essere coinvolta nel sonno.
Sembrava fatta, no? GluClα nei neuroni dFB regola il sonno. E invece… sorpresa! Usando altri driver specifici per i neuroni dFB, il silenziamento di GluClα non aveva alcun effetto sul sonno. Com’era possibile? Studi recenti avevano suggerito che forse non tutti i neuroni marcati da 23E10-GAL4 nel cervello fossero rilevanti per il sonno, ma che questo driver marcasse anche neuroni importanti nel cordone nervoso ventrale (VNC), l’equivalente della nostra medula spinale.
Abbiamo quindi usato dei “trucchetti” genetici per escludere l’espressione nel cervello (usando Otd-FLP) o specificamente nei neuroni dFB (usando vGluT-trojan-GAL80 o Tsh-GAL80). E voilà! Silenziando GluClα solo nel VNC (escludendo il cervello o i dFB), il sonno notturno diminuiva ancora! Quindi, il ruolo cruciale di GluClα non era nel cervello (almeno non nei dFB), ma nel VNC.
Identikit dei Neuroni del Sonno nel VNC
Il driver 23E10-GAL4 marca diverse coppie di neuroni nel VNC. Sapevamo già di una coppia di “neuroni promotori del sonno” (VNC-SP) e una coppia di “neuroni di proiezione del gusto” (TPN1). Abbiamo testato se GluClα fosse importante in questi, ma silenziarlo specificamente lì non cambiava il sonno. Però, il driver 23E10 marca anche altre due coppie di neuroni nel VNC, con i corpi cellulari localizzati nel neuromero metatoracico.
Abbiamo isolato geneticamente queste due coppie di neuroni e provato a silenziare GluClα solo in loro. Risultato? Drammatica riduzione del sonno notturno! Erano proprio loro i neuroni chiave in cui GluClα doveva funzionare. Questi neuroni, quando li abbiamo attivati artificialmente (con un canale del sodio batterico, NaChBac), facevano dormire meno i moscerini. Questo confermava il loro ruolo regolatorio: la loro attività promuove la veglia, quindi la loro inibizione (mediata da GluClα) promuove il sonno.
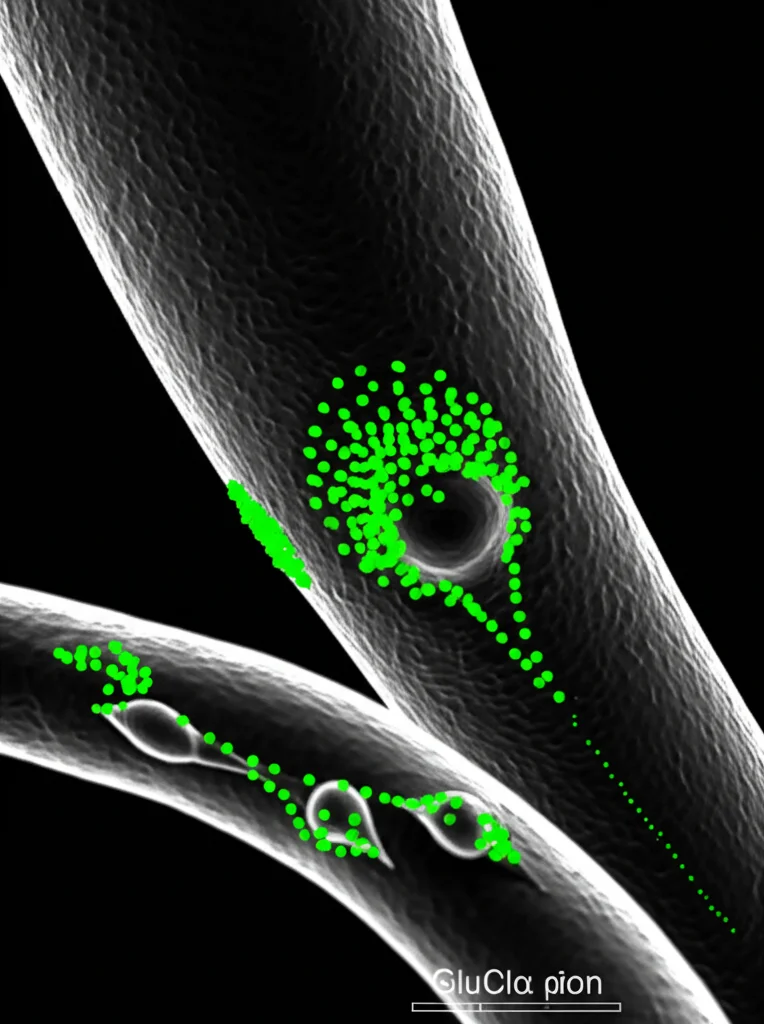
Come Funziona l’Interruttore GluClα?
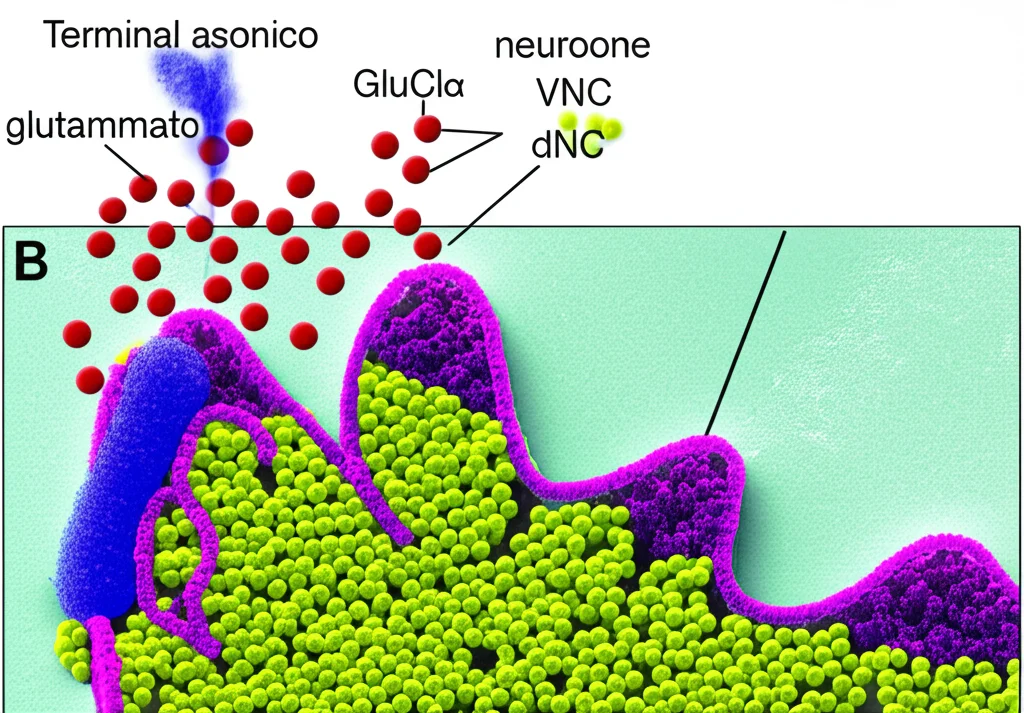
GluClα è un canale per gli ioni cloruro. Quando il glutammato si lega, il canale si apre, fa entrare ioni cloruro negativi nella cellula e questo tende a iperpolarizzare il neurone, rendendolo meno eccitabile. È un meccanismo inibitorio. Per vederlo in azione, abbiamo usato una tecnica di imaging del calcio (con GCaMP7s) direttamente su queste due coppie di neuroni nel VNC mentre spruzzavamo glutammato vicino a loro. Abbiamo osservato una rapida e robusta riduzione dei livelli di calcio intracellulare, segno che l’attività neuronale veniva inibita. Quando invece abbiamo ripetuto l’esperimento in moscerini dove GluClα era stato silenziato in questi neuroni, l’effetto inibitorio del glutammato era quasi scomparso. Questo dimostra che GluClα media proprio l’input inibitorio del glutammato su questi neuroni del VNC.
Connessioni e Significato: Un Quadro Più Ampio
Ma da dove arriva il segnale del glutammato a questi neuroni del VNC? E dove mandano il loro segnale questi neuroni? Abbiamo studiato la loro morfologia: i corpi cellulari sono nel VNC (nel metatorace), ma i loro assoni si estendono sia nel VNC (fino al mesotorace) sia su fino al cervello, in una regione chiamata ganglio sottoesofageo (SOG). Usando marcatori per le sinapsi, abbiamo visto che i segnali in uscita (presinaptici) sono lungo queste proiezioni, mentre i segnali in entrata (postsinaptici) sembrano essere ricevuti principalmente vicino al corpo cellulare, nel VNC.
Con una tecnica chiamata GRASP, che fa illuminare le sinapsi attive tra due popolazioni neuronali, abbiamo confermato che questi neuroni del VNC ricevono effettivamente contatti sinaptici diretti da neuroni glutammatergici proprio lì, vicino ai loro corpi cellulari. Abbiamo anche confermato con un’altra strategia genetica che GluClα è espresso proprio in questi neuroni del VNC marcati da 23E10.
Il quadro che emerge è questo: due coppie specifiche di neuroni nel VNC ricevono un segnale inibitorio dal glutammato attraverso il recettore GluClα. Questa inibizione è necessaria per promuovere il sonno notturno. Questi neuroni, a loro volta, proiettano verso il cervello (SOG), probabilmente trasmettendo informazioni relative allo stato di sonno/veglia.
Cosa Ci Insegna Tutto Questo?
Questa scoperta è affascinante per diversi motivi.
- Rivela un ruolo inaspettato e inibitorio del glutammato nella promozione del sonno in *Drosophila*, sfidando l’idea che sia solo un neurotrasmettitore “sveglia”.
- Identifica un meccanismo specifico (GluClα) e una popolazione neuronale precisa (le due coppie di neuroni nel VNC) cruciali per questo processo.
- Sottolinea l’importanza del VNC, spesso trascurato negli studi sul sonno che si concentrano sul cervello, come centro di integrazione e regolazione del sonno.
- Apre nuove strade per capire come diversi segnali (magari provenienti dalla periferia o dal cervello stesso) vengano integrati a livello del VNC per controllare il nostro bisogno di dormire.
- Interessante notare che GluClα è omologo ai recettori della glicina nei mammiferi, anch’essi canali del cloruro inibitori importanti, specialmente nel midollo spinale. Studiare GluClα nei moscerini potrebbe quindi darci indizi anche sul funzionamento di questi sistemi nei mammiferi, inclusi noi umani.
Insomma, il piccolo moscerino della frutta ci ha ancora una volta mostrato quanto possa essere complesso e sorprendente il controllo di un comportamento apparentemente semplice come il sonno. La prossima volta che vedrete un moscerino ronzare, pensate che dentro di sé nasconde circuiti neurali incredibilmente sofisticati che stiamo solo iniziando a decifrare! E chissà quali altri segreti ci rivelerà in futuro…
Fonte: Springer