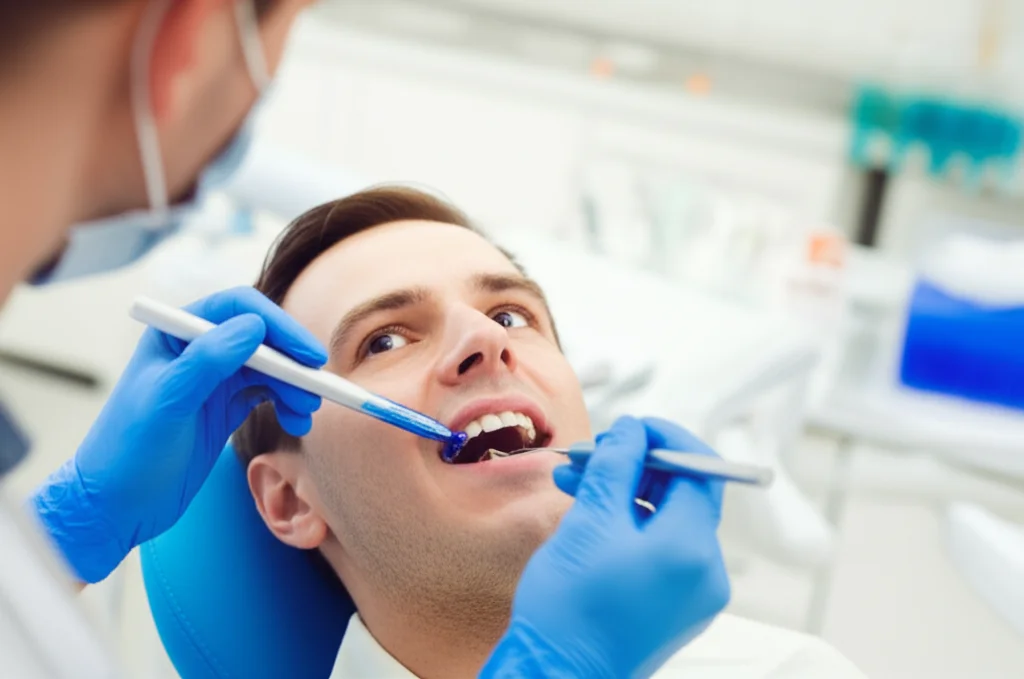
Blu di Metilene Appiccicoso: La Mia Scommessa per Annientare i Super-Batteri dal Dentista!
Ehilà, appassionati di scienza e curiosi! Oggi voglio raccontarvi di una sfida che mi sta particolarmente a cuore e che potrebbe cambiare le carte in tavola nel mondo dell’odontoiatria. Parliamo di batteri, di quelli tosti, quelli che se ne fregano degli antibiotici e ci causano un sacco di problemi. Ebbene sì, la resistenza antimicrobica è un osso duro, un problema globale che ci costringe a trovare nuove armi. Pensate che, solo negli Stati Uniti, più di 35.000 persone muoiono ogni anno per infezioni resistenti agli antibiotici. E i dentisti? Beh, anche noi facciamo la nostra parte, prescrivendo circa il 10% di tutti gli antibiotici a livello mondiale. Urge un cambio di rotta!
Una Luce in Fondo al Tunnel: la Terapia Fotodinamica Antimicrobica (aPDT)
Da un po’ di tempo, nel mio laboratorio e in tanti altri centri di ricerca, stiamo esplorando una strategia super affascinante: la terapia fotodinamica antimicrobica, o aPDT. Immaginatela come un attacco di precisione: usiamo una sostanza speciale, chiamata fotosensibilizzatore (PS), la luce e l’ossigeno per fare letteralmente la pelle ai microbi cattivi. È un metodo non invasivo, sicuro e, udite udite, non sembra creare nuovi super-batteri resistenti!
Tra i vari fotosensibilizzatori, il mio “campione” è il blu di metilene (MB). È una vecchia conoscenza della medicina, sicuro e non tossico. Studi in vitro (cioè in laboratorio, nelle provette) dimostrano che è una bomba contro batteri Gram-positivi e Gram-negativi, funghi (come la fastidiosissima Candida albicans) e persino protozoi. Sembra perfetto, no?
Il Problema: Quando il Blu di Metilene Fa i Capricci
Purtroppo, c’è un “ma”. Nonostante i successi in provetta, quando passiamo alla pratica clinica, cioè sulla poltrona del dentista, i risultati non sono sempre all’altezza delle aspettative. Perché? Principalmente per due motivi:
- Scarsa ritenzione: Il blu di metilene, di solito usato in soluzione acquosa, viene lavato via troppo in fretta dalla saliva. È come cercare di dipingere sotto la pioggia!
- Aggregazione: Il blu di metilene tende ad “appallottolarsi”, formando aggregati. In questa forma, la sua capacità di produrre le specie reattive dell’ossigeno (ROS), quelle che uccidono i microbi, diminuisce drasticamente. Le molecole singole (monomeri) sono molto più efficaci, soprattutto nel generare il temibile ossigeno singoletto.
Alcuni colleghi hanno provato ad aumentare la concentrazione di MB o ad abbinarlo ad altre sostanze, ma la strada è ancora in salita. L’aggregazione è influenzata da tanti fattori: il mezzo in cui si trova, la concentrazione, il pH. Noi, nel mio gruppo di ricerca, abbiamo già visto che usare un surfattante come il Sodio Dodecil Solfato (SDS) aiuta a tenere le molecole di MB separate e felici.
La Mia Idea “Viscosa”: Un Gel per Vincere la Sfida
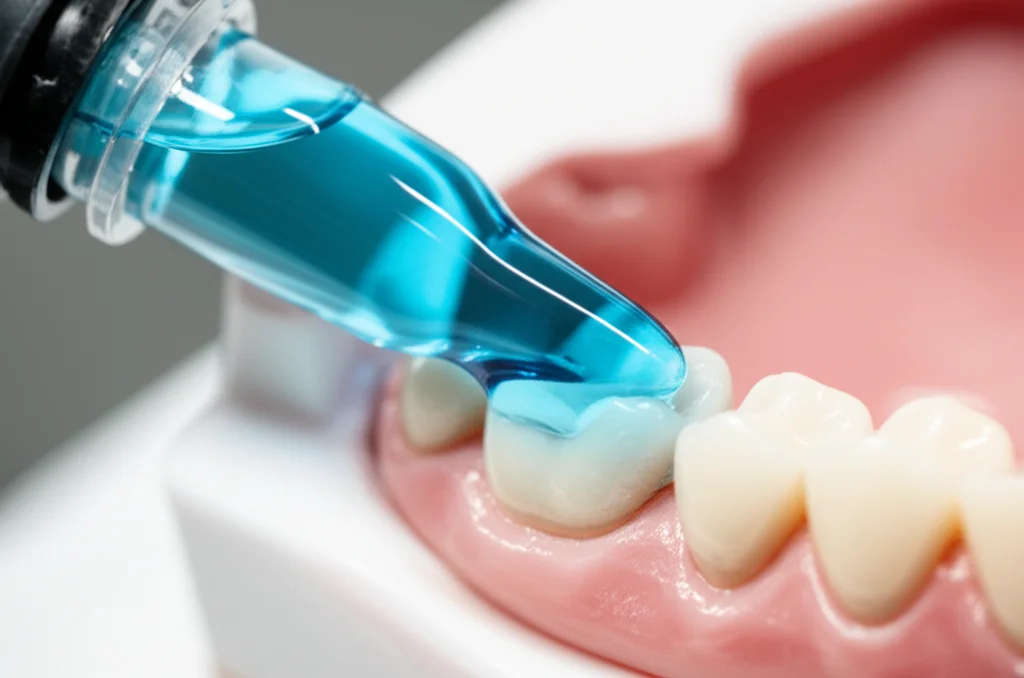
Ed ecco che mi è venuta l’illuminazione (è il caso di dirlo, parlando di aPDT!): e se rendessimo il blu di metilene più… appiccicoso? Più viscoso? Un gel, per intenderci. L’idea è semplice: una formulazione più densa dovrebbe rimanere più a lungo sul sito da trattare, resistendo al flusso salivare e permettendo al fotosensibilizzatore di fare il suo lavoro.
Per questo, ci siamo messi all’opera per sviluppare una formulazione di blu di metilene ad alta viscosità, pensata apposta per l’uso dentistico. Non solo più viscosa, ma anche studiata per minimizzare l’aggregazione del MB.
Come abbiamo fatto? Abbiamo giocato con diversi ingredienti:
- Polimeri mucoadesivi: Sostanze come l’idrossipropilmetilcellulosa (HPMC) e la carbossimetilcellulosa (CMC). Sono derivati della cellulosa che, oltre ad aumentare la viscosità, hanno la bella proprietà di “attaccarsi” alle mucose, prolungando il tempo di contatto. La CMC, in particolare, è già usata nei dentifrici.
- Un surfattante (SDS): Come dicevo prima, aiuta a prevenire l’aggregazione del MB.
- pH acido: Abbiamo scoperto che un ambiente acido aiuta a mantenere il MB in forma monomerica, più attiva.
- Concentrazioni ridotte di MB: Anche questo contribuisce a limitare l’aggregazione.
L’obiettivo era trovare il giusto equilibrio per avere una consistenza ideale per l’applicazione e la permanenza in bocca, senza che il prodotto venisse neutralizzato subito dalla saliva.
I Risultati: Stabilità e Attività Antimicrobica Promettenti
Dopo vari tentativi e aggiustamenti, abbiamo messo a punto una formulazione che ci ha dato grandi soddisfazioni. Abbiamo testato la stabilità per un anno intero: le sue proprietà (aspetto, odore, pH, contenuto di MB) sono rimaste invariate. Un piccolo aumento dell’aggregazione si è visto tra i 6 e i 12 mesi, ma talmente minimo da non compromettere, a nostro avviso, l’efficacia. Certo, la viscosità è un po’ diminuita dopo 3 anni, ma chi terrebbe una preparazione galenica per così tanto tempo?
E l’efficacia? Qui la cosa si fa interessante. Abbiamo testato la nostra formulazione su biofilm di Candida albicans, un fungo che forma delle vere e proprie fortezze difficili da espugnare. Abbiamo notato che, rispetto al blu di metilene in acqua, la nostra formulazione viscosa veniva assorbita un po’ meno dalle cellule del biofilm. Uno potrebbe pensare: “Ah, allora funziona meno!”. E invece no! L’attività antimicrobica in vitro è risultata comparabile a quella del MB in acqua. La nostra ipotesi? La minore aggregazione del MB nella nostra formula compensa il minor assorbimento, permettendo una produzione più efficiente di ossigeno singoletto, il killer dei microbi.
Abbiamo anche visto che il pH acido (intorno a 5) era il migliore per ridurre l’aggregazione, e che il polimero anionico CMC (allo 0.5%) in combinazione con SDS (allo 0.25%) e una concentrazione di MB dello 0.005% dava i risultati più equilibrati tra viscosità e riduzione dell’aggregazione.
Il Doppio Trattamento: Due Colpi Sono Meglio di Uno!
Un’altra scoperta intrigante riguarda la modalità di applicazione. Abbiamo confrontato un singolo trattamento di illuminazione lungo (54 minuti) con un doppio trattamento (due cicli da 27 minuti, con una nuova applicazione di fotosensibilizzatore tra un ciclo e l’altro). Ebbene, il doppio trattamento si è rivelato nettamente superiore, con una riduzione dei microbi di circa 4 Log (cioè 10.000 volte!), mentre il trattamento singolo più lungo ha dato una riduzione di solo 1 Log.
Questo suggerisce che “stressare” i microbi con applicazioni successive è più efficace. Forse il primo trattamento indebolisce le difese del biofilm, permettendo al secondo di penetrare più a fondo e fare piazza pulita. Questa strategia potrebbe essere vincente anche in clinica, dove la saliva tende a diluire il prodotto.
Cosa Significa Tutto Questo per il Futuro dell’Odontoiatria?
Sono davvero entusiasta di questi risultati! Aver sviluppato una formulazione di blu di metilene viscosa che mantiene la sua efficacia antimicrobica, ma che promette una migliore applicazione e ritenzione in bocca, è un passo avanti importante. Potrebbe rendere la aPDT una pratica clinica più semplice, affidabile e, speriamo, più diffusa per combattere le infezioni orali, specialmente quelle resistenti ai farmaci.
Certo, la strada è ancora lunga. Dovremo studiare meglio le proprietà mucoadesive, ottimizzare i parametri di illuminazione per l’uso clinico e, ovviamente, passare ai test sull’uomo. Ma la base che abbiamo costruito è solida.
La lotta contro i super-batteri è una maratona, non uno sprint. Ma con un po’ di ingegno, perseveranza e un pizzico di “viscosità”, sono convinto che potremo offrire ai pazienti cure sempre più efficaci e sicure. E chissà, forse un giorno diremo addio a molte delle infezioni che oggi ci danno tanto filo da torcere!
Fonte: Springer