Carcinoma Epatocellulare: Smascherato il Trio Maligno YY1-USP13-WWP1 che Guida il Tumore!
Ciao a tutti! Oggi voglio parlarvi di un argomento che mi sta particolarmente a cuore e che riguarda una battaglia che molti combattono silenziosamente: quella contro il carcinoma epatocellulare (HCC). Pensate, è il sesto tumore più diffuso al mondo e la terza causa di morte per cancro. Numeri che fanno riflettere, vero? Soprattutto in paesi come la Cina, la situazione è ancora più critica.
Il problema principale dell’HCC è che spesso si nasconde, non dà sintomi chiari all’inizio, e quando finalmente viene scoperto, solo una piccola percentuale di pazienti (circa il 30%) può accedere a cure potenzialmente risolutive come la chirurgia. Per tutti gli altri, si apre la strada di terapie mirate e immunoterapie, sperando di rendere il tumore operabile. Nonostante i progressi, la prognosi rimane spesso infausta. Ecco perché è fondamentale scavare a fondo nei meccanismi molecolari che guidano la progressione di questo tumore. Capire come funziona ci permette di identificare nuovi bersagli e, speriamo, sviluppare terapie più efficaci.
L’Intricato Mondo dell’Ubiquitinazione: Etichette Molecolari per le Proteine
Entriamo un po’ nel tecnico, ma cercherò di renderlo semplice e affascinante. Avete mai sentito parlare di ubiquitinazione? Immaginate delle minuscole etichette molecolari (l’ubiquitina) che vengono attaccate alle proteine dentro le nostre cellule. Queste etichette sono come dei post-it che dicono alla proteina cosa fare: “Ehi tu, devi essere degradata!”, oppure “Cambia funzione!”, o ancora “Spostati!”. È un processo fondamentale per regolare tantissime attività cellulari, dal ciclo di vita della cellula alla riparazione del DNA.
Questo “etichettamento” avviene grazie a una squadra di enzimi (E1, E2, E3). Ma, come in ogni sistema ben regolato, c’è anche chi toglie queste etichette: sono gli enzimi deubiquitinanti (DUBs). Loro fanno il lavoro opposto, rimuovendo l’ubiquitina e controllando così il destino delle proteine. È un equilibrio delicatissimo!
USP13: Un Attore Chiave (e Ambiguo) nel Dramma del Cancro
Tra le centinaia di DUBs conosciuti, oggi ci concentriamo su uno in particolare: USP13 (Ubiquitin-specific protease 13). Questo enzima è coinvolto in un sacco di processi cellulari, dal metabolismo energetico all’autofagia (una specie di “pulizia” interna della cellula).
Studi precedenti hanno mostrato che USP13 può avere un ruolo ambivalente nei tumori. A volte agisce come un promotore del cancro:
- Nel cancro gastrico, stabilizza una proteina (Ciclina D1) che favorisce la crescita cellulare.
- Nei tumori ovarici, aiuta a stabilizzare enzimi chiave per il metabolismo delle cellule tumorali.
- In altri casi, può addirittura indurre resistenza a farmaci come l’imatinib.
Altre volte, però, USP13 sembra avere un ruolo protettivo:
- Nel cancro al seno e alla vescica, può stabilizzare una proteina oncosoppressore chiamata PTEN, frenando lo sviluppo del tumore.
Insomma, USP13 è un personaggio complesso, il cui ruolo dipende molto dal contesto e dai suoi “partner” molecolari.
La Scoperta: USP13 è Sovraespresso nell’HCC e Predice Sfortuna
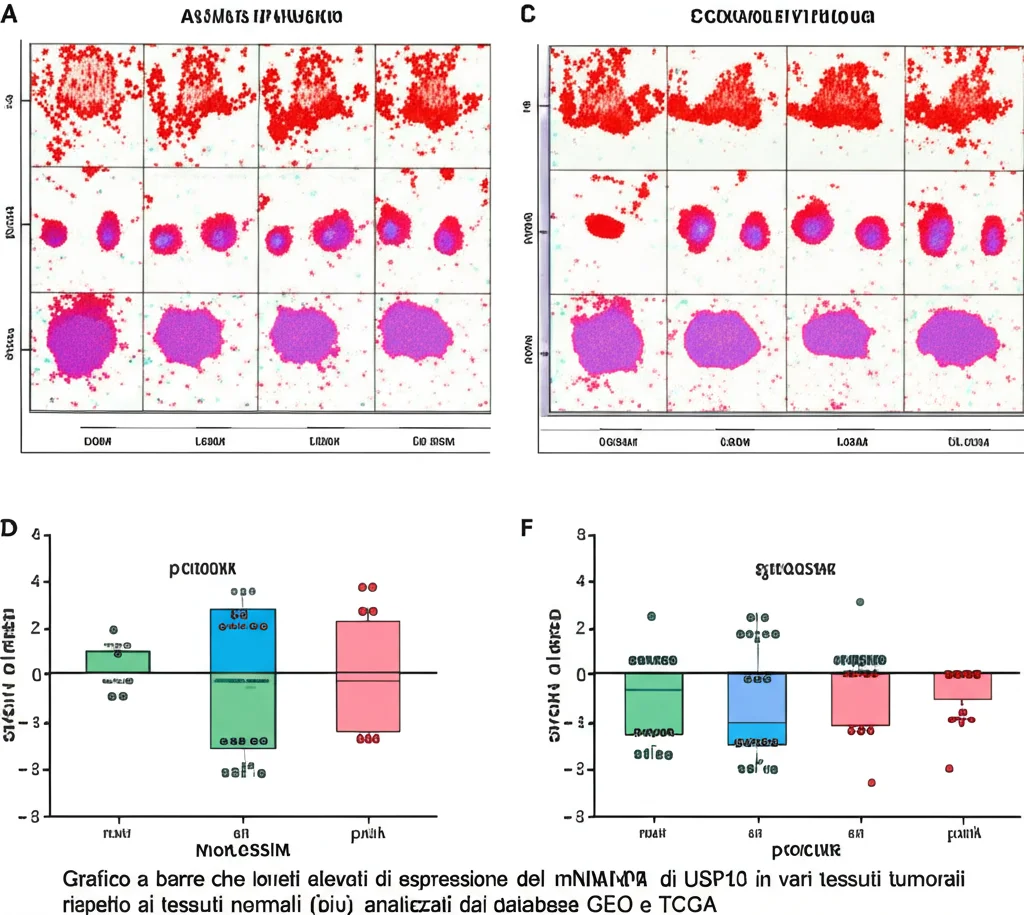
Cosa fa USP13 nel carcinoma epatocellulare? Analizzando dati da grandi database pubblici (come GEO e TCGA) e campioni di tessuto tumorale reali, abbiamo fatto una scoperta importante: USP13 è significativamente più abbondante nelle cellule tumorali del fegato rispetto ai tessuti sani circostanti. Non solo, i pazienti con livelli più alti di USP13 tendono ad avere una prognosi peggiore (sopravvivenza globale, sopravvivenza specifica per malattia e intervallo libero da progressione più brevi) e tumori di dimensioni maggiori. Abbiamo persino creato un nomogramma (uno strumento predittivo) che, includendo i livelli di USP13, aiuta a stimare il rischio per i pazienti. Anche nelle linee cellulari di HCC che usiamo in laboratorio, abbiamo confermato questa iperespressione di USP13. Sembra proprio che USP13 sia un fattore di rischio nell’HCC.
USP13 all’Opera: Un Acceleratore della Malignità
Ok, USP13 è alto nell’HCC. Ma cosa fa concretamente? Per capirlo, abbiamo fatto degli esperimenti “spegnendo” (knockdown) o “accendendo” (sovraespressione) il gene USP13 in cellule di HCC in coltura. I risultati sono stati chiari:
- Spegnendo USP13: Le cellule tumorali crescevano meno (sia come numero che come capacità di formare colonie), migravano più lentamente (come visto negli esperimenti di “wound healing” e Transwell) e perdevano parte delle loro caratteristiche “staminali” (la capacità di formare sferoidi e l’espressione di proteine legate alla staminalità come c-Myc, Nanog, Lin28B diminuivano).
- Accendendo USP13: Ottenevamo l’effetto opposto! Le cellule proliferavano di più, migravano più velocemente e mostravano caratteristiche staminali potenziate.
Questi esperimenti, sia in vitro che poi confermati in vivo su modelli animali, ci dicono che USP13 agisce come un oncogene nell’HCC, promuovendo attivamente i comportamenti maligni delle cellule tumorali.
Il Compare di USP13: WWP1 Entra in Scena
Ma come fa USP13 a fare tutto questo? Sospettavamo che non agisse da solo. Abbiamo quindi cercato i suoi “partner” molecolari. Utilizzando tecniche come la co-immunoprecipitazione (Co-IP), abbiamo pescato un nuovo compagno di USP13: una proteina chiamata WWP1 (WW domain–containing ubiquitin E3 ligase 1). WWP1 è un enzima E3, cioè uno di quelli che attaccano le etichette di ubiquitina! Sembra un paradosso, vero? Un “pulitore” (USP13) che si lega a un “etichettatore” (WWP1).
Abbiamo confermato questa interazione in vari modi, anche vedendo che le due proteine si trovano spesso insieme (colocalizzano) nel nucleo delle cellule tumorali. Abbiamo persino identificato le parti specifiche di USP13 (i domini UBP e UBA, ma non il dominio USP) che sono cruciali per legarsi a WWP1.
Il Meccanismo Svelato: USP13 Salva WWP1 dalla Distruzione
Ora la domanda clou: perché USP13 si lega a WWP1? La nostra ipotesi era che USP13, essendo un DUB, potesse “pulire” WWP1 dalle etichette di ubiquitina che ne causano la degradazione, stabilizzandolo. E avevamo ragione!
- Quando spegnevamo USP13, i livelli della proteina WWP1 diminuivano drasticamente (ma non il suo RNA, indicando un effetto post-traduzionale).
- Quando accendevamo USP13, i livelli di WWP1 aumentavano.
- Esperimenti specifici sull’ubiquitinazione hanno mostrato che USP13 riduceva proprio le etichette di ubiquitina attaccate a WWP1.
- Abbiamo scoperto che USP13 rimuove specificamente le catene di ubiquitina legate ai residui di lisina K29 e K48 di WWP1. Queste sono spesso segnali per la degradazione tramite il proteasoma (il sistema di “smaltimento rifiuti” della cellula).
- Infatti, bloccando il proteasoma (con un inibitore chiamato MG132), riuscivamo a impedire la degradazione di WWP1 causata dalla mancanza di USP13. Bloccando invece i lisosomi (un altro sistema di degradazione, con HCQ), non ottenevamo lo stesso effetto.
Quindi, USP13 protegge WWP1 dalla degradazione via proteasoma, rimuovendo le sue etichette di ubiquitina K29 e K48.
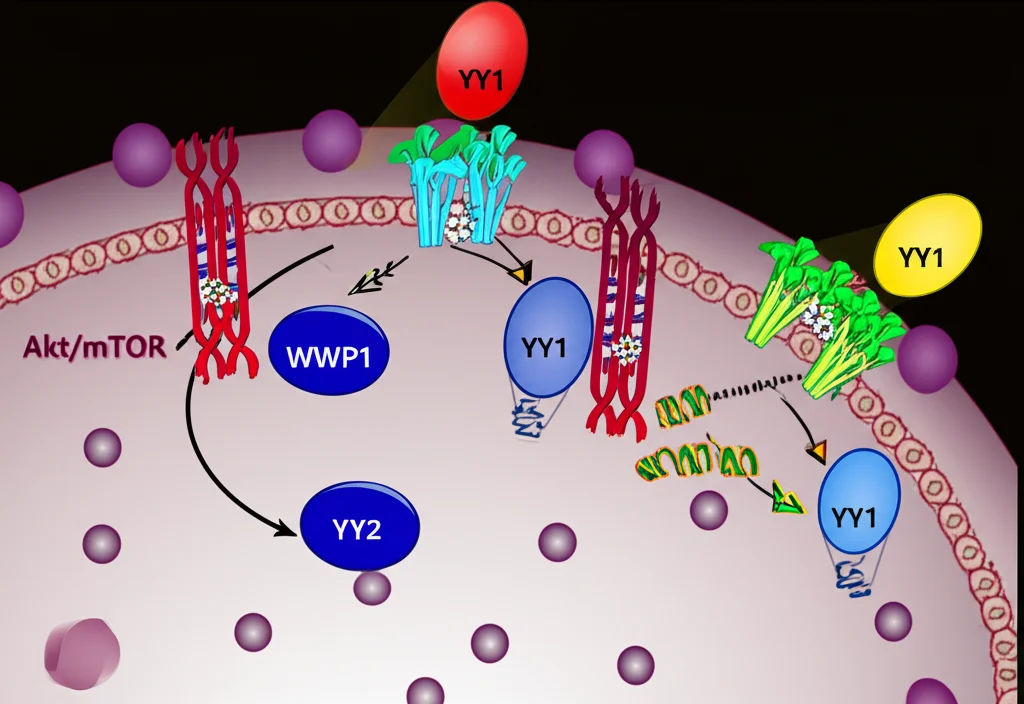
L’Effetto a Cascata: WWP1 Attiva la Via Akt/mTOR
Ok, USP13 stabilizza WWP1. E quindi? Sappiamo da studi precedenti che WWP1, pur essendo un E3 ligase, può attivare indirettamente una via di segnalazione cellulare molto importante per la crescita e la sopravvivenza delle cellule tumorali: la via Akt/mTOR. Lo fa modulando l’attività di PTEN (anche se nel nostro studio, come in altri, non abbiamo visto cambiamenti nei livelli totali di PTEN, ma nella sua attività sì).
Abbiamo verificato se questo accadesse anche nel nostro contesto:
- Spegnendo USP13, non solo diminuiva WWP1, ma si riduceva anche l’attivazione di Akt e mTOR (misurata dai loro livelli fosforilati, p-Akt e p-mTOR).
- Se in queste cellule “prive” di USP13 reintroducevamo WWP1, l’attivazione di Akt/mTOR veniva ripristinata!
- Viceversa, nelle cellule con tanto USP13 (e quindi tanto WWP1 e via Akt/mTOR attiva), se spegnevamo WWP1, l’attivazione di Akt/mTOR diminuiva.
Questo dimostra che USP13 attiva la via Akt/mTOR proprio attraverso la stabilizzazione di WWP1. E questa attivazione è cruciale per gli effetti oncogenici di USP13: se bloccavamo la via Akt/mTOR (con un farmaco chiamato Rapamicina), l’aumento di proliferazione, migrazione e staminalità indotto da USP13 veniva annullato o ridotto.
Il Mandante: YY1 Accende l’Interruttore di USP13
Ma c’è un ultimo pezzo del puzzle. Chi dice a USP13 di essere così abbondante nelle cellule tumorali? Abbiamo cercato i fattori di trascrizione (proteine che regolano l’espressione dei geni) che potessero controllare il gene di USP13. Utilizzando database bioinformatici e analisi di correlazione, un candidato è emerso con forza: YY1 (Yin Yang 1).
YY1 è un fattore di trascrizione noto per essere spesso iperattivo in molti tumori, incluso l’HCC. Abbiamo scoperto che:
- I livelli di YY1 e USP13 sono fortemente correlati nei tumori HCC.
- Spegendo YY1 nelle cellule tumorali, diminuivano sia l’RNA che la proteina USP13. Accendendolo, aumentavano.
- Con esperimenti di ChIP (Immunoprecipitazione della Cromatina) e Luciferase Reporter Assay, abbiamo dimostrato che YY1 si lega direttamente a una specifica regione (chiamata motif 3) nel promotore del gene USP13, attivandone la trascrizione. La sequenza precisa a cui si lega è AAAAATAGCGTC.
Quindi, YY1 è il “mandante” che ordina una maggiore produzione di USP13.

L’Asse Completo: YY1 → USP13 → WWP1 → Akt/mTOR
Ora abbiamo il quadro completo! Abbiamo identificato un asse di segnalazione oncogenico:
YY1 (il fattore di trascrizione) attiva l’espressione di USP13 (l’enzima deubiquitinante), che a sua volta stabilizza WWP1 (l’E3 ligase) rimuovendo le sue etichette di ubiquitina (K29/K48). WWP1 stabilizzato attiva poi la via Akt/mTOR, promuovendo la proliferazione, la migrazione e la staminalità delle cellule di carcinoma epatocellulare.
Abbiamo confermato questa catena di eventi anche con esperimenti di “salvataggio”: se spegnevamo YY1 (riducendo USP13 e WWP1), ma poi forzavamo l’espressione di USP13, riuscivamo a ripristinare i livelli di WWP1 e a contrastare gli effetti anti-tumorali dello spegnimento di YY1. Questo dimostra che YY1 esercita i suoi effetti pro-tumorali in gran parte proprio attraverso USP13.
Conferme sul Campo (Anzi, nel Topo!) e Implicazioni Terapeutiche
Per essere sicuri che tutto questo non fosse solo un gioco di molecole in provetta, siamo passati ai modelli animali. Abbiamo iniettato cellule di HCC modificate in topi nude (senza sistema immunitario, per non rigettare le cellule umane):
- I topi iniettati con cellule in cui USP13 era stato spento sviluppavano tumori significativamente più piccoli rispetto ai controlli.
- I topi iniettati con cellule che sovraesprimevano USP13 sviluppavano tumori più grandi.
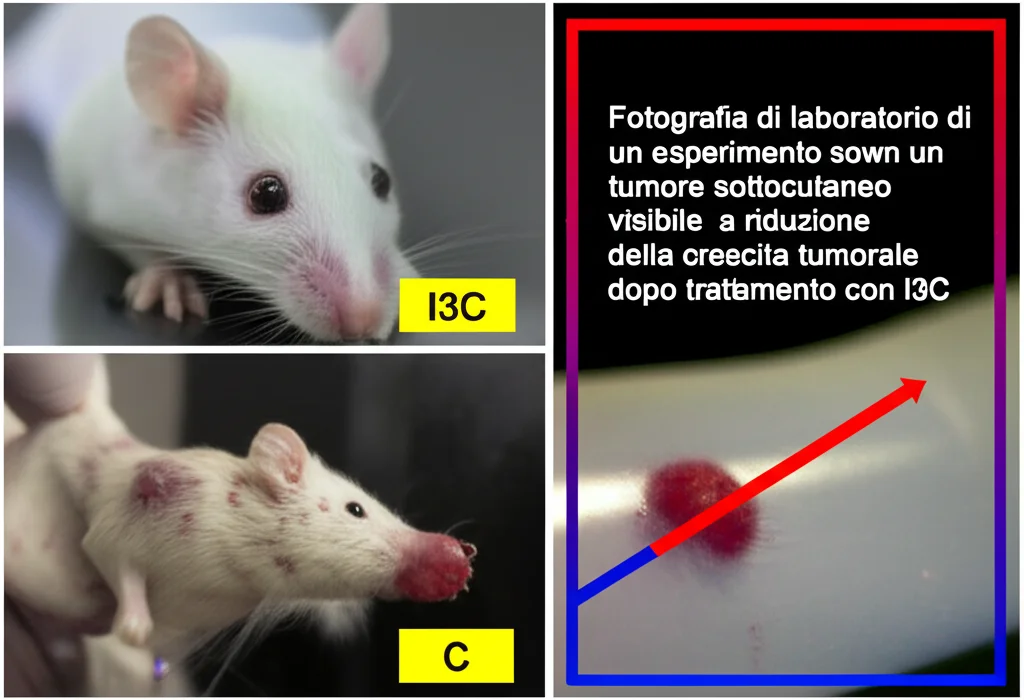
- E qui la prova del nove: se trattavamo i topi con tumori indotti da USP13 alto con una sostanza chiamata Indole-3-carbinolo (I3C) – un composto naturale trovato nelle crucifere e noto per inibire WWP1 – la crescita tumorale veniva significativamente rallentata!
Analizzando i tumori dei topi, abbiamo confermato che i livelli delle proteine (Ki67 come marcatore di proliferazione, USP13, WWP1) seguivano esattamente lo schema che ci aspettavamo in base all’asse YY1/USP13/WWP1.
Conclusioni: Una Nuova Strada per Colpire l’HCC?
Questa ricerca, secondo me, è davvero entusiasmante! Abbiamo svelato un meccanismo molecolare prima sconosciuto, l’asse YY1/USP13/WWP1, che agisce come un potente motore per la progressione del carcinoma epatocellulare attivando la via Akt/mTOR. Abbiamo identificato WWP1 come un nuovo substrato di USP13 e chiarito come YY1 regoli trascrizionalmente USP13.
La cosa più importante è che questo asse rappresenta un potenziale bersaglio terapeutico. Colpire uno qualsiasi dei componenti di questa catena (YY1, USP13 o WWP1) potrebbe essere una strategia efficace per frenare l’HCC. L’esperimento con l’I3C (inibitore di WWP1) nei topi è un primo passo promettente in questa direzione.
Certo, la strada è ancora lunga. Serviranno studi più ampi, magari su coorti di pazienti più grandi e diversificate, per validare ulteriormente questi risultati e capire come tradurli in terapie concrete. Ma aver identificato questo “trio maligno” è un passo avanti significativo nella comprensione e, speriamo, nella lotta contro questo terribile tumore.
Fonte: Springer