Artrosi e Staminali: La Sorpresa dai Ratti che Apre Nuove Strade (e Qualche Domanda!)
Ciao a tutti! Oggi voglio parlarvi di un argomento che mi appassiona tantissimo e che riguarda molti di noi, direttamente o indirettamente: l’artrosi. Sapete, quella fastidiosa malattia degenerativa delle articolazioni che porta al consumo della cartilagine e a un bel po’ di infiammazione. Un problema comune, che peggiora con l’età e che, diciamocelo, limita parecchio la qualità della vita.
Alla Ricerca di Nuove Soluzioni: Entrano in Scena le Staminali
Da tempo la ricerca medica esplora nuove strade per combattere l’artrosi, perché le terapie attuali (farmaci, fisioterapia, perdita di peso) spesso danno solo un sollievo temporaneo e non riparano davvero il danno. Una delle frontiere più promettenti è quella della medicina rigenerativa, e in particolare l’uso delle cellule staminali mesenchimali (MSC).
Tra queste, quelle derivate dal tessuto adiposo, le cosiddette ASCs (Adipose-derived Stromal Cells), sono particolarmente interessanti. Perché? Perché sembrano avere delle capacità fantastiche: possono “sentire” dove c’è un danno, migrare lì e rilasciare un cocktail di molecole bioattive (il famoso secretoma) che fa un sacco di cose utili:
- Modula la risposta immunitaria, riducendo l’infiammazione.
- Aiuta le cellule staminali residenti nel tessuto a sopravvivere e proliferare.
- Favorisce la formazione di nuovi vasi sanguigni (angiogenesi).
- Contribuisce al rimodellamento della matrice extracellulare.
Insomma, sembrano le candidate ideali per riparare i tessuti danneggiati, come la cartilagine nell’artrosi. Diversi studi preclinici e clinici hanno già mostrato risultati incoraggianti con iniezioni intra-articolari di ASCs, riportando riduzione del dolore e persino segni di rigenerazione della cartilagine.
L’Idea: Potenziare le ASCs e Usare il Loro “Succo”
C’è un però. Sembra che le ASCs non funzionino tanto perché si trasformano direttamente in cellule della cartilagine (condrociti), ma più per i segnali che inviano, per le sostanze che rilasciano (effetto paracrino). Questo ha fatto nascere un’idea: e se usassimo direttamente il loro “succo”, il secretoma, invece delle cellule intere? Questo approccio, detto cell-free, potrebbe avere vantaggi: meno rischi legati al sistema immunitario e forse più facilità di produzione e conservazione.
Inoltre, per rendere le ASCs ancora più “potenti” nel produrre questo secretoma benefico, si è pensato di “stimolarle” in laboratorio. Una sostanza promettente per questo “priming” è il lisato piastrinico umano (hPL), un prodotto derivato dalle piastrine del sangue che, in vitro, aiuta le cellule a crescere meglio, a rimanere giovani più a lungo e ad aumentare la loro attività secretoria.

L’Esperimento sui Ratti: Cosa Volevamo Scoprire
Ed eccoci al cuore della ricerca che vi racconto oggi. Abbiamo voluto testare proprio questo: l’effetto delle ASCs umane (stimolate con hPL) e del loro secretoma (SEC) su un modello di artrosi indotta nei ratti. L’ipotesi era che le ASCs “potenziate” con hPL fossero più efficaci nel combattere l’artrosi, e volevamo vedere se il loro secretoma da solo potesse fare lo stesso lavoro, magari anche meglio e con più sicurezza.
Quindi, abbiamo preso delle ASCs umane da tessuto adiposo (ottenuto da donatrici sane consenzienti, ovviamente nel rispetto di tutte le norme etiche), le abbiamo coltivate e “caricate” con hPL. Una parte di queste cellule è stata usata per preparare il secretoma: dopo il priming con hPL, le cellule sono state messe in un terreno senza siero per 48 ore per raccogliere tutte le sostanze da loro rilasciate.
Nel frattempo, abbiamo indotto l’artrosi nel ginocchio di alcuni ratti maschi (usando una sostanza chiamata monoiodoacetato di sodio, MIA, un metodo standard). Dopo 14 giorni, quando l’artrosi si era instaurata, abbiamo diviso i ratti in tre gruppi:
- Gruppo di controllo (CTRL): ha ricevuto un’iniezione di soluzione salina.
- Gruppo Secretoma (SEC): ha ricevuto un’iniezione del secretoma preparato.
- Gruppo ASCs: ha ricevuto un’iniezione delle cellule ASCs preparate (1 milione di cellule per ginocchio).
Abbiamo seguito i ratti per cinque settimane, monitorando il loro peso e stato di salute generale. Alla fine, abbiamo esaminato le loro articolazioni al microscopio (analisi istologica) per vedere lo stato della cartilagine e dell’osso sottostante, usando un sistema di punteggio standardizzato (OARSI) per quantificare il danno. Abbiamo anche cercato tracce delle cellule umane iniettate tramite immunoistochimica.
I Risultati: Una Sorpresa Inaspettata!
E qui arriva il colpo di scena. Ci aspettavamo che le ASCs, e forse il secretoma, migliorassero la situazione rispetto al gruppo di controllo. Invece, è successo qualcosa di molto diverso.
Innanzitutto, dal punto di vista clinico, nessun ratto ha avuto complicazioni e tutti sono aumentati di peso normalmente, segno che i trattamenti erano ben tollerati a livello generale.
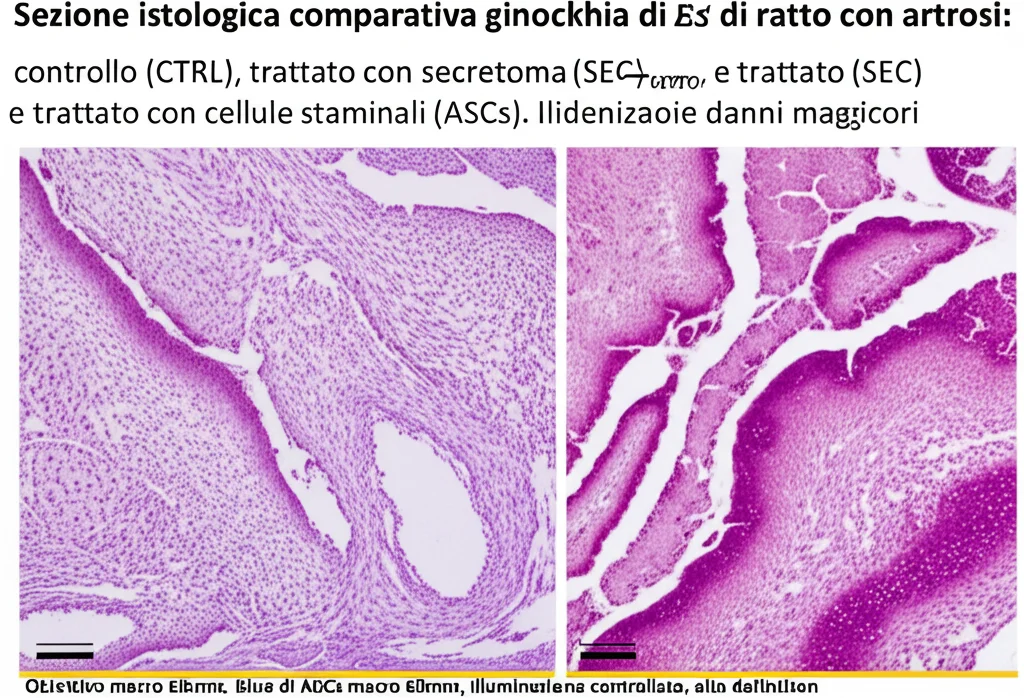
Ma guardando le articolazioni al microscopio… sorpresa! Il gruppo trattato con le cellule ASCs ha mostrato un danno articolare significativamente peggiore rispetto al gruppo di controllo. L’analisi istologica ha rivelato necrosi della cartilagine più severa, deplezione marcata di GAG (i componenti fondamentali della matrice cartilaginea), rimodellamento dell’osso subcondrale e persino ispessimento della capsula articolare con formazione di osteofiti. Un risultato decisamente contrario alle aspettative!
E il gruppo trattato con il secretoma (SEC)? Qui i risultati sono stati più “neutri”. Il danno articolare era simile a quello del gruppo di controllo (CTRL), con degenerazione della cartilagine da lieve a moderata. Non c’è stato un peggioramento come con le cellule, ma nemmeno un miglioramento significativo rispetto alla semplice soluzione salina. Statisticamente, non c’era differenza tra il gruppo SEC e il gruppo CTRL.
Infine, l’analisi immunoistochimica non ha rilevato cellule umane (marcate con MHCI umano) nelle articolazioni dei ratti dopo 5 settimane, né nel gruppo di controllo né in quello trattato con ASCs. Questo non è del tutto sorprendente, perché è probabile che le cellule xenogeniche (umane in un ospite ratto) vengano eliminate dal sistema immunitario dell’ospite nel giro di qualche settimana.
Cosa Può Essere Successo? Ipotesi e Implicazioni
Questo risultato inatteso con le ASCs ci ha fatto riflettere molto. L’ipotesi più probabile è che l’iniezione di cellule umane in un ratto immunocompetente (cioè con un sistema immunitario funzionante) abbia scatenato una reazione immunitaria avversa. Anche se non abbiamo visto segni clinici evidenti di infiammazione acuta e l’istologia mostrava solo infiammazione minima occasionale, è possibile che questa risposta immunitaria xenogenica abbia contribuito al peggioramento della patologia articolare, mascherando eventuali effetti benefici delle cellule. Il fatto che il secretoma, essendo acellulare, non abbia causato lo stesso peggioramento supporta questa idea: il problema sembra legato proprio alla presenza delle cellule “straniere”.
È vero che altri studi hanno usato cellule umane in modelli animali immunocompetenti con risultati positivi, ma le condizioni sperimentali possono variare molto (tipo di cellule, preparazione, modello di malattia, ecc.). Ad esempio, alcuni studi usavano ASCs autologhe (dello stesso animale) o sistemi di coltura 3D che potrebbero ridurre l’immunogenicità. I nostri risultati sono più in linea con alcuni lavori, come quello di Warmink et al., che hanno osservato un peggioramento dell’artrosi dopo iniezione di MSC umane in un modello di ratto.
Questo studio sottolinea quindi la complessità delle terapie cellulari, specialmente quando si usano cellule xenogeniche. Il sistema immunitario dell’ospite gioca un ruolo cruciale e non va sottovalutato, anche in siti considerati relativamente “immuno-privilegiati” come l’articolazione.
Il Secretoma: Una Strada Ancora Aperta?
E il secretoma? Beh, il fatto che non abbia peggiorato la situazione è già una buona notizia, suggerendo che possa essere un’alternativa più sicura rispetto alle cellule intere in un contesto xenogenico. Tuttavia, in questo specifico esperimento, non ha mostrato un’efficacia rigenerativa chiara rispetto al controllo.
Questo non significa che il secretoma sia inutile. Potrebbe essere una questione di dosaggio, di composizione (magari il priming con hPL non era ottimale o la raccolta del secretoma andava affinata) o di variabilità biologica tra gli animali. C’è ancora molto da studiare per capire come ottimizzare la preparazione del secretoma e sfruttare al meglio il suo potenziale terapeutico. La ricerca sulle vescicole extracellulari e altri componenti del secretoma è in pieno fermento e rappresenta una frontiera molto promettente per terapie cell-free.
In Conclusione: Tante Domande, Nuove Prospettive
Quindi, cosa ci portiamo a casa da questa ricerca? Principalmente, la consapevolezza che la biologia è complessa e non sempre le cose vanno come ci aspettiamo!
- L’uso di cellule staminali umane (ASCs) in un modello animale immunocompetente può portare a risultati inattesi, probabilmente a causa di reazioni immunitarie che possono peggiorare la patologia.
- Il secretoma derivato da queste cellule sembra essere meglio tollerato e più sicuro da questo punto di vista, non avendo causato peggioramenti.
- Tuttavia, nel nostro setting sperimentale, il secretoma non ha mostrato chiari benefici rigenerativi rispetto al controllo.
Questo non ferma la ricerca, anzi! Apre nuove domande e indica direzioni future: studiare più a fondo le interazioni immunitarie, testare le ASCs in modelli animali immunodeficienti per valutarne il potenziale intrinseco senza il “disturbo” immunitario, e soprattutto, continuare a esplorare e ottimizzare le terapie basate sul secretoma, caratterizzandone meglio i componenti attivi e le condizioni ottimali per la sua produzione ed efficacia.
La strada verso una cura rigenerativa per l’artrosi è ancora lunga e piena di sfide, ma ogni studio, anche quelli con risultati sorprendenti come questo, aggiunge un tassello importante alla nostra conoscenza. E io non vedo l’ora di scoprire cosa ci riserverà il futuro!
Fonte: Springer