Alcol e Intestino: Quel Legame Pericoloso che Accende l’Infiammazione (Anche a Basse Dosi!)
Ciao a tutti! Oggi voglio parlarvi di qualcosa che tocca le vite di molti: il rapporto tra alcol e il nostro corpo, ma da una prospettiva un po’ diversa dal solito. Non parleremo solo di fegato o “sbornia”, ma scenderemo più in profondità, fino al nostro intestino e alle cellule immunitarie. Siete pronti a scoprire come anche un consumo apparentemente moderato di alcol possa mettere a soqquadro il nostro organismo in modi che forse non immaginate?
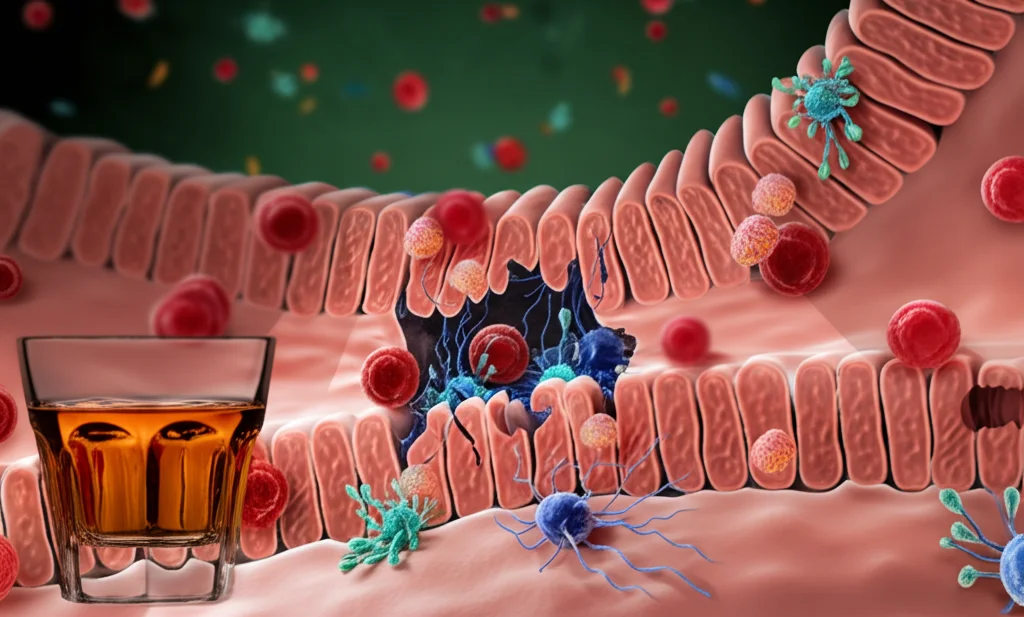
Partiamo da un concetto chiave: la permeabilità intestinale, o come la chiamano gli scienziati, “leaky gut”. Immaginate la parete del vostro intestino come una fitta rete di sicurezza, fatta di cellule (gli enterociti) tenute insieme da giunzioni strettissime (le tight junctions). Questa barriera è super selettiva: fa passare i nutrienti ma blocca tossine, batteri cattivi e altre molecole indesiderate. L’alcol, purtroppo, è un po’ un vandalo per questa barriera.
La Doppia Azione Dannosa dell’Alcol
Il guaio è che l’alcol agisce su due fronti:
- Danno Diretto: L’alcol e il suo metabolita principale, l’acetaldeide (una sostanza piuttosto tossica), possono danneggiare direttamente le cellule intestinali e allentare quelle giunzioni strette. Pensate a delle piccole crepe che si aprono nella rete di sicurezza. Questo avviene in parte a causa dello stress ossidativo (la produzione di radicali liberi, molecole instabili che danneggiano le cellule).
- Danno Indiretto via Disbiosi: L’alcol altera l’equilibrio del nostro microbiota intestinale, quell’ecosistema complesso di batteri, funghi e altri microrganismi che vive nel nostro intestino. Questo squilibrio, chiamato disbiosi, favorisce la crescita di batteri potenzialmente dannosi a scapito di quelli benefici. E indovinate un po’? Un microbiota alterato può contribuire ulteriormente a danneggiare la barriera intestinale.
Questione di Dosi: Non Tutto l’Alcol è Uguale (Ma Fa Danno Comunque)
Ora, potreste pensare: “Ok, ma questo vale solo per chi beve molto?”. Beh, la ricerca su cui si basa questo articolo (condotta su topi, che metabolizzano l’alcol diversamente da noi, quindi le dosi non sono direttamente paragonabili, ma i meccanismi sì!) ha messo a confronto una dose “bassa” e una “alta” di alcol, somministrate per 16 settimane.
I risultati sono affascinanti e un po’ preoccupanti. La dose alta (che nei topi portava a un tasso alcolemico nel sangue paragonabile a uno stato di ubriachezza conclamata nell’uomo, circa 0.15%) causava danni evidenti al fegato (aumento degli enzimi epatici, accumulo di grasso, stress ossidativo, apoptosi – morte cellulare programmata) e una chiara disbiosi intestinale. In particolare, si è vista una riduzione dei batteri buoni come i Lachnospiraceae e un aumento di altri, come gli Alistipes spp. (su cui torneremo).
E la dose bassa (che portava a un tasso alcolemico più simile a una leggera euforia, circa 0.05-0.06%)? Anche qui c’erano segni di danno al fegato, seppur più lievi (aumento dell’apoptosi e dell’accumulo di grasso e stress ossidativo, ma senza alterare significativamente gli enzimi epatici o il peso del fegato). Ma la cosa più interessante è che anche la bassa dose causava un aumento della permeabilità intestinale (leaky gut)! La disbiosi, invece, era molto meno evidente o quasi assente rispetto al gruppo di controllo.
Leaky Gut: Quando la Barriera Cede
Come hanno fatto a vedere questo “leaky gut”? Hanno usato diversi metodi:
- FITC-Dextran: Hanno dato ai topi una molecola fluorescente (FITC-dextran) che normalmente non dovrebbe passare la barriera intestinale. Trovarla nel sangue significa che la barriera è “bucata”. E l’hanno trovata in entrambi i gruppi trattati con alcol, anche se in misura maggiore nel gruppo ad alta dose.
- Endotossine (LPS): Hanno misurato i livelli di LPS nel sangue. L’LPS è un componente della parete dei batteri Gram-negativi. La sua presenza nel sangue (endotossiemia) è un chiaro segno di leaky gut. Anche qui, entrambi i gruppi alcolici mostravano livelli elevati.
- Beta-Glucano: Simile all’LPS, ma è un componente della parete dei funghi. Era elevato solo nel gruppo ad alta dose, suggerendo forse un danno più severo o una diversa composizione del microbiota fungino.
- Occludina: Hanno visualizzato direttamente l’occludina, una delle proteine chiave delle giunzioni strette, nell’intestino. Era ridotta in entrambi i gruppi alcolici, ma di più in quello ad alta dose.
Insomma, la barriera intestinale soffre anche con basse dosi di alcol cronico. E quando la barriera cede, cosa succede?
Disbiosi e Infiammazione Sistemica: Un Circolo Vizioso
Il leaky gut permette a frammenti batterici (come LPS e beta-glucano) e altre molecole infiammatorie di passare dall’intestino al flusso sanguigno. Questo scatena una risposta immunitaria sistemica. Le nostre cellule immunitarie, in particolare i macrofagi, riconoscono questi “intrusi” e si attivano, rilasciando citochine pro-infiammatorie (come TNF-α e IL-6).
Infatti, lo studio ha mostrato un aumento di queste citochine infiammatorie nel sangue dei topi trattati con alcol, in modo più marcato nel gruppo ad alta dose. Questa infiammazione sistemica cronica di basso grado è collegata a un sacco di problemi di salute, dall’aterosclerosi alle malattie autoimmuni, fino a peggiorare le malattie epatiche.
E la disbiosi? Come detto, era evidente solo nel gruppo ad alta dose. Hanno visto un calo dei Firmicutes (in particolare Lachnospiraceae, spesso associati a un intestino sano) e un aumento dei Bacteroidota (in particolare Alistipes spp.). Il ruolo di Alistipes è complesso: a volte protettivo, altre volte associato a infiammazione e persino a depressione o cancro del colon-retto. Il suo aumento con alte dosi di alcol merita sicuramente più attenzione.
La Crisi Energetica Cellulare: Alcol vs Mitocondri
Ma come fa l’alcol a causare tutto questo a livello cellulare? Qui entra in gioco un altro meccanismo affascinante: l’interferenza con il metabolismo energetico delle cellule. Lo studio ha esaminato cosa succede quando si espongono direttamente cellule intestinali (Caco-2) e macrofagi (RAW264.7) all’alcol in laboratorio.
Hanno scoperto che l’alcol danneggia i mitocondri, le “centrali energetiche” delle nostre cellule. Usando una tecnica chiamata analisi del flusso extracellulare, hanno visto che l’alcol riduce il consumo di ossigeno (OCR), un indicatore della respirazione mitocondriale. Questo avviene sia negli enterociti che nei macrofagi. L’acetaldeide prodotta dal metabolismo dell’alcol è particolarmente tossica per i mitocondri.
Quando i mitocondri sono in difficoltà, le cellule cercano un’alternativa per produrre energia: aumentano la glicolisi, un processo meno efficiente che non richiede ossigeno (misurato come aumento del tasso di acidificazione extracellulare, ECAR). Questo “switch glicolitico” è interessante perché è spesso associato a uno stato pro-infiammatorio, specialmente nei macrofagi.
Infatti, sia le cellule intestinali che i macrofagi esposti all’alcol mostravano non solo mitocondri danneggiati e aumento della glicolisi, ma anche un aumento dell’espressione di geni infiammatori (come NF-κB, IL-8 negli enterociti; IL-1β, iNOS nei macrofagi). Nelle cellule intestinali, questo si traduceva anche in una ridotta integrità della barriera (misurata come TEER, resistenza elettrica transepiteliale). E tutto questo avveniva in modo dose-dipendente: concentrazioni più alte di alcol causavano un aumento maggiore della glicolisi e dell’infiammazione.

Leaky Gut Prima della Disbiosi?
Un punto chiave che emerge da questa ricerca è che il leaky gut sembra essere più sensibile all’alcol rispetto alla disbiosi. Anche la dose bassa, che non causava alterazioni significative nel microbiota fecale, induceva comunque un aumento della permeabilità intestinale e infiammazione sistemica.
Questo suggerisce che il danno diretto dell’alcol alla barriera intestinale (forse mediato proprio dall’interferenza mitocondriale e dallo shift glicolitico) potrebbe essere uno dei primi eventi scatenati dal consumo cronico, anche a livelli considerati “bassi” o “moderati”. La disbiosi, invece, potrebbe richiedere dosi più elevate o un’esposizione più prolungata per manifestarsi in modo evidente, ma quando arriva, peggiora ulteriormente la situazione.
Cosa Portiamo a Casa?
Insomma, questa ricerca ci dipinge un quadro complesso ma chiaro: l’alcol, anche a dosi non estreme, può innescare una cascata di eventi dannosi partendo dall’intestino.
- Danneggia direttamente la barriera intestinale e interferisce con l’energia delle cellule (mitocondri KO, glicolisi ON).
- Questo porta a leaky gut (aumento della permeabilità).
- A dosi più alte, altera significativamente il microbiota (disbiosi), peggiorando il leaky gut.
- Il leaky gut fa passare molecole batteriche nel sangue.
- L’alcol assorbito e le molecole batteriche attivano i macrofagi (sempre con mitocondri KO e glicolisi ON), promuovendo uno stato pro-infiammatorio.
- Questa infiammazione sistemica può contribuire a una miriade di problemi di salute a lungo termine.
La scoperta che il leaky gut possa precedere una disbiosi manifesta è particolarmente importante. Potrebbe significare che i danni iniziano prima di quanto pensiamo e che misurare la permeabilità intestinale potrebbe essere un indicatore più sensibile dei danni precoci da alcol rispetto alla sola analisi del microbiota.
Ovviamente, si tratta di studi su modelli animali e cellulari, e servono conferme sull’uomo. Ma il messaggio è forte e chiaro: il nostro intestino è un organo incredibilmente sensibile agli effetti dell’alcol, e le conseguenze possono andare ben oltre un semplice mal di pancia. Forse è ora di riconsiderare quel bicchiere “innocente” con un po’ più di consapevolezza per la salute del nostro prezioso intestino.
Fonte: Springer