Adenocarcinoma Pancreatico: Decifrare il Labirinto Immunitario con la Genetica per Accendere l’Immunoterapia
Ciao a tutti! Oggi voglio portarvi in un viaggio affascinante nel cuore di una delle sfide più ardue dell’oncologia moderna: l’adenocarcinoma duttale pancreatico, o PDAC. È un nemico ostico, lo sappiamo bene, soprattutto perché tende a resistere alle armi più innovative che abbiamo sviluppato, come l’immunoterapia basata sugli inibitori dei checkpoint immunitari (ICI). Ma perché questa resistenza? E, soprattutto, come possiamo superarla?
Il Microambiente Tumore: Una Fortezza da Espugnare
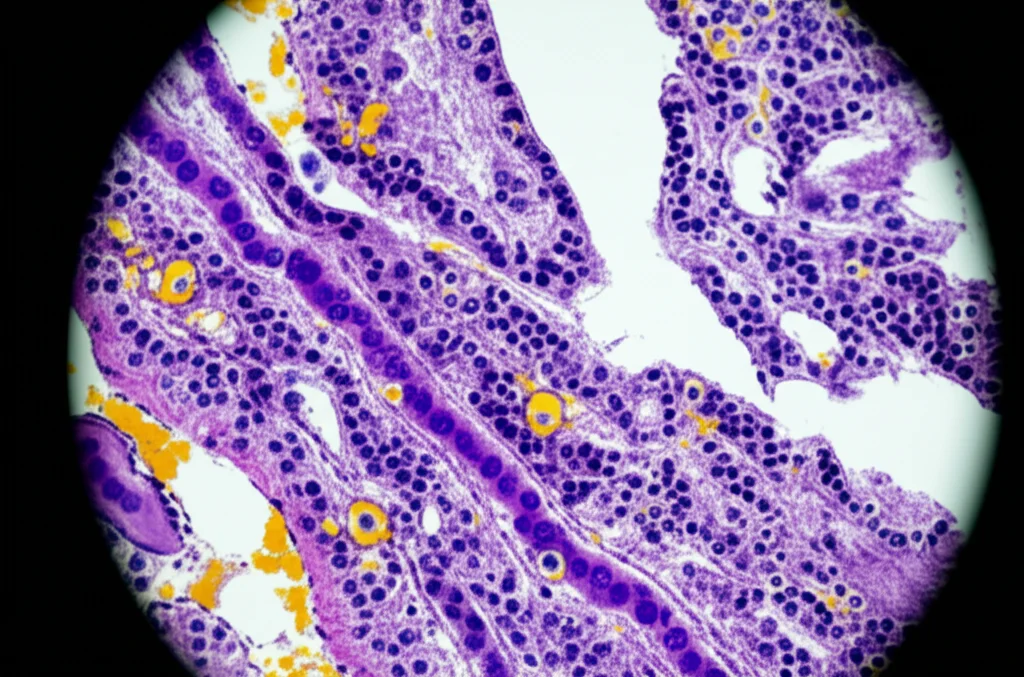
Immaginate il tumore al pancreas non come una massa isolata, ma come una città fortificata. Questa fortezza è il suo microambiente tumorale (TME): un complesso ecosistema fatto di cellule tumorali, vasi sanguigni, matrice fibrosa densa (lo stroma) e, crucialmente, cellule immunitarie. Il problema è che nel PDAC, questo TME è profondamente immunosoppressivo. In pratica, il tumore riesce a “corrompere” o silenziare le cellule immunitarie che dovrebbero attaccarlo, creando uno scudo protettivo.
Pensate a un processo chiamato immunoediting: il sistema immunitario all’inizio magari prova a combattere, eliminando le cellule tumorali più riconoscibili (immunogeniche). Ma così facendo, seleziona involontariamente cloni tumorali più “furbi”, meno visibili al sistema immunitario, che prendono il sopravvento. È una sorta di selezione naturale al contrario, che rende il tumore sempre più resistente. L’immunoterapia, che funziona magnificamente in altri tumori “risvegliando” il sistema immunitario, qui trova le porte sbarrate.
Le cellule chiave in questa battaglia sono i linfociti T citotossici CD8+, i nostri soldati d’élite anti-cancro. Purtroppo, nel TME del PDAC, la loro efficacia è spesso compromessa. A peggiorare le cose ci sono i macrofagi associati al tumore (TAM), che possono passare da un ruolo potenzialmente protettivo a uno che favorisce la crescita tumorale. Insomma, un ambiente davvero complicato!
Fattori Esterni ed Interni: Un Intreccio Complesso
Ma non è solo una questione di cellule immunitarie locali. La loro funzione è influenzata da un sacco di altri fattori:
- Fattori infiammatori: L’infiammazione cronica, spesso presente nel PDAC, può paradossalmente aiutare il tumore, reclutando cellule immunosoppressive e inibendo quelle “buone”. Citochine come IL-6 e IL-10 gettano benzina sul fuoco.
- Metaboliti: Le sostanze prodotte dal metabolismo cellulare, sia del tumore che del nostro corpo, possono influenzare l’attività immunitaria.
- Microbiota intestinale: Ebbene sì, i batteri che ospitiamo nel nostro intestino hanno un ruolo! La loro composizione può modulare la risposta immunitaria sistemica e influenzare l’efficacia delle terapie, inclusa l’immunoterapia. Una disbiosi (squilibrio del microbiota) può peggiorare l’infiammazione e l’immunosoppressione.
Capire come tutti questi elementi interagiscono è fondamentale per trovare nuove strategie. Ed è qui che entra in gioco uno strumento statistico potentissimo: la Randomizzazione Mendeliana (MR).
La Randomizzazione Mendeliana: Usare la Genetica come Esperimento Naturale
Vi spiego in modo semplice. La MR è un metodo ingegnoso che usa le nostre varianti genetiche (piccole differenze nel DNA ereditate casualmente, come i Polimorfismi a Singolo Nucleotide o SNP) come se fossero degli “strumenti” per studiare le relazioni causa-effetto tra un’esposizione (es. un certo tipo di cellula immunitaria, un batterio, un metabolita) e un esito (il rischio di PDAC). Poiché queste varianti genetiche sono assegnate alla nascita, prima che si sviluppino malattie o intervengano fattori confondenti (come lo stile di vita), la MR ci aiuta a capire se un certo fattore *causa* realmente un effetto, e non è solo associato per caso o a causa di altri fattori nascosti.
Nel nostro studio, abbiamo usato enormi database di associazioni genome-wide (GWAS) che collegano milioni di SNP a migliaia di tratti diversi:
- Oltre 700 tipi di cellule immunitarie circolanti.
- Centinaia di specie batteriche intestinali e loro vie metaboliche.
- Decine di proteine infiammatorie circolanti.
- Più di mille metaboliti nel sangue.
Abbiamo applicato metodi MR sofisticati (come l’Inverse Variance Weighted – IVW, ma anche altri più robusti come il cML-MA per controllare la “pleiotropia”, cioè quando una variante genetica influenza più cose contemporaneamente) per vedere se ci fossero legami causali tra questi tratti e il rischio di PDAC.
Cosa Abbiamo Scoperto? Un Panorama Immunitario Sfumato
I risultati sono stati illuminanti e ci offrono una visione molto più dettagliata del “terreno immunologico” del PDAC.
1. Cellule Immunitarie: Abbiamo trovato associazioni suggestive con 22 diversi fenotipi di cellule immunitarie. La tendenza generale? Una riduzione di molti tipi di monociti (come i CD14+CD16-) e di diverse popolazioni di linfociti B (come le cellule B naive-mature o quelle IgD+). Questo potrebbe indicare che il PDAC contribuisce attivamente a “spegnere” o ridurre queste importanti difese. Tuttavia, non è tutto negativo: abbiamo visto un aumento dell’associazione con alcune sottopopolazioni di linfociti T, in particolare la percentuale di cellule T CD8+ memoria centrale, e anche con le cellule che esprimono CD38 (CD38+ su cellule CD3- CD19-). Questi potrebbero essere potenziali bersagli o indicatori importanti. Anche le cellule dendritiche hanno mostrato una tendenza alla diminuzione, mentre le cellule mieloidi soppressorie (MDSC), note per il loro ruolo pro-tumorale, sembravano diminuire in questo contesto genetico, un dato interessante da approfondire.

2. Microbiota Intestinale: Il legame con i batteri intestinali è emerso chiaramente. Abbiamo trovato associazioni significative con 8 tratti batterici (dopo aver escluso quelli potenzialmente confusi dalla pleiotropia). In particolare, il genere Collinsella sembra associato a un aumento del rischio/associazione con PDAC, mentre Ruminococcus torques sembra associato a una diminuzione. Anche specifiche vie metaboliche batteriche (legate alla fermentazione del piruvato o alla degradazione del lattosio) hanno mostrato legami. Questo rafforza l’idea che il nostro microbiota influenzi l’immunità e la patogenesi del PDAC.
3. Fattori Infiammatori: Anche qui, dati intriganti. Livelli geneticamente più alti della subunità beta dell’Interleuchina-12 (IL-12β) sono risultati associati a un aumento del rischio/associazione, mentre livelli più alti della glicoproteina di superficie CD5 dei linfociti T erano associati a una diminuzione. L’IL-12 è una citochina complessa, spesso pro-infiammatoria e anti-tumorale, ma qui il suo ruolo sembra più sfumato. CD5 è un marcatore importante sui linfociti T, e la sua riduzione potrebbe avere implicazioni funzionali.
4. Metaboliti nel Sangue: Una valanga di dati! Dopo un’attenta analisi per escludere associazioni spurie, sono rimasti 31 metaboliti con associazioni robuste. Alcuni erano associati a una diminuzione del rischio (es. 2-idrossipalmitato, palmitoleoilcarnitina), altri a un aumento (es. il rapporto Ornitina/fosfato, arabitolo/xilitolo). Questo apre scenari affascinanti su come il metabolismo sistemico possa influenzare lo sviluppo del PDAC.
Collegare i Punti: Come Batteri, Infiammazione e Metaboliti Parlano alle Cellule Immunitarie
La parte forse più eccitante è stata cercare di capire come questi diversi “strati” biologici interagiscono. Abbiamo usato la MR per vedere se i batteri, i fattori infiammatori o i metaboliti associati al PDAC potessero influenzare *causalmente* proprio quei 22 tratti di cellule immunitarie che avevamo identificato come legati al tumore.
E abbiamo trovato delle connessioni! Per esempio:
- Collinsella sembra aumentare l’espressione di CD64 (un recettore importante per la risposta anticorpale) su un tipo di monociti.
- Ruminococcus torques sembra ridurre l’espressione di CCR2 (un recettore chiave per il richiamo dei monociti) e aumentare l’espressione di CD39 (un enzima immunosoppressivo) sui linfociti T CD4+.
- L’IL-12β ha mostrato un ruolo complesso, associata sia a una riduzione del numero di alcune cellule B, sia a un aumento dell’espressione di CD19 (marcatore di attivazione) su altre cellule B.
- I livelli di CD5 sembrano ridurre la percentuale di quelle cellule T CD8+ memoria centrale che avevamo visto aumentate in associazione al PDAC.
- Diversi metaboliti (come il rapporto fosfato/fosfoetanolamina o il 4-idrossiippurato) sono risultati associati a cambiamenti nell’espressione di marcatori sui monociti (CCR2, CD11b) o sull’espressione di CD38.
Questi risultati iniziano a dipingere un quadro di come il microbiota, l’infiammazione sistemica e il metabolismo possano plasmare il panorama immunitario nel contesto del PDAC, influenzando potenzialmente la sua progressione e la risposta alle terapie.

Implicazioni e Prossimi Passi: Verso un’Immunoterapia Personalizzata?
Questo studio, pur con i suoi limiti (si basa su dati genetici, principalmente europei, e le associazioni sono suggestive, non prove definitive di causalità), ci fornisce indizi preziosi. Ci aiuta a capire meglio perché il PDAC è così resistente all’immunoterapia e suggerisce nuove strade:
- Identificare nuovi bersagli terapeutici: I tratti immunitari, batterici, infiammatori o metabolici che abbiamo identificato potrebbero diventare bersagli per nuove terapie.
- Biomarcatori predittivi: Alcuni di questi tratti potrebbero aiutarci a predire quali pazienti potrebbero rispondere meglio a certe terapie.
- Strategie combinate: Forse la chiave è combinare l’immunoterapia con approcci che modulano il microbiota intestinale o specifiche vie metaboliche.
- Immunoterapia personalizzata: Comprendere il profilo immunologico e metabolico individuale potrebbe portare a trattamenti più mirati.
Certo, la strada è ancora lunga. Questi risultati devono essere validati con studi sperimentali e clinici. Dobbiamo capire i meccanismi esatti dietro queste associazioni e considerare altri fattori come l’ambiente e lo stile di vita. Ma aver usato la potenza della genetica e della randomizzazione mendeliana per gettare luce su questo complesso panorama è un passo avanti importante. Ci offre una mappa più dettagliata per navigare il difficile terreno del PDAC e, speriamo, per sviluppare strategie più efficaci per combatterlo. La ricerca non si ferma!
Fonte: Springer