Cuore Affaticato? Una Nuova Speranza dall’Acido Nitro-Oleico per l’HFpEF!
Ciao a tutti! Oggi voglio parlarvi di un argomento che mi sta molto a cuore, letteralmente: lo scompenso cardiaco a frazione di eiezione preservata, meglio conosciuto come HFpEF. Sembra un nome complicato, vero? In pratica, si tratta di una condizione in cui il cuore, pur pompando sangue in modo apparentemente normale (la famosa “frazione di eiezione” è conservata), fa una fatica tremenda a rilassarsi tra un battito e l’altro. Questo porta a sintomi come affanno, stanchezza e ridotta capacità di fare esercizio fisico.
Il problema è che l’HFpEF sta diventando sempre più comune, soprattutto nelle popolazioni più anziane dei paesi occidentali, e spesso è legato a doppio filo con altri disturbi come l’ipertensione e la sindrome metabolica (pensate a obesità, insulino-resistenza…). E la cosa frustrante? Le opzioni terapeutiche specifiche ed efficaci scarseggiano. Certo, abbiamo visto qualche progresso con gli inibitori SGLT2, ma c’è ancora tanta strada da fare per colpire direttamente il malfunzionamento cardiaco.
La Sfida dell’HFpEF Cardiometabolico
Concentriamoci un attimo sul sottogruppo di pazienti con HFpEF definito “cardiometabolico”. Qui troviamo spesso obesità, sindrome metabolica, infiammazione vascolare sistemica e ipertensione. Un bel mix, non c’è che dire. Il cuore di questi pazienti subisce un vero e proprio “rimodellamento metabolico”: fa fatica a gestire i grassi, sviluppa insulino-resistenza e non riesce più ad adattare il suo consumo energetico alle necessità variabili.
Pensate che il cuore, per funzionare, ha bisogno di energia (ATP). Questa energia la ricava principalmente bruciando acidi grassi (FAO) o glucosio (GO). Nell’HFpEF, questo equilibrio si altera, spesso sbilanciandosi verso un eccessivo utilizzo di grassi, il che però richiede più ossigeno e può portare all’accumulo di intermedi lipidici tossici (lipotossicità), danneggiando ulteriormente le cellule cardiache e i loro motori energetici: i mitocondri.
Entra in Scena l’Acido Nitro-Oleico (NO2-OA)
Ed è qui che entra in gioco una molecola affascinante: l’acido nitro-oleico (NO2-OA). Si tratta di un acido grasso “modificato”, un prodotto naturale che si forma nel nostro corpo durante risposte metaboliche e infiammatorie. Studi precedenti avevano già suggerito che il NO2-OA potesse avere effetti positivi sulle sindromi metaboliche, migliorando la tolleranza al glucosio e la funzione delle cellule adipose.
La domanda che ci siamo posti è stata: potrebbe questa molecola aiutare anche il cuore affetto da HFpEF? Per scoprirlo, abbiamo utilizzato un modello animale molto realistico: topolini sottoposti a una dieta ricca di grassi (HFD) e a un trattamento cronico con L-NAME, un inibitore che blocca la produzione di ossido nitrico endoteliale, mimando così sia la componente metabolica che quella ipertensiva dell’HFpEF umano.
Dopo 11 settimane, questi topolini sviluppavano tutti i segni dell’HFpEF: cuore ipertrofico, fibrosi, e soprattutto una chiara disfunzione diastolica (il cuore faticava a rilassarsi). A questo punto, per le successive 4 settimane, abbiamo trattato un gruppo di questi topi con NO2-OA.
Risultati Sorprendenti: Il Cuore Torna a Rilassarsi!
I risultati sono stati davvero incoraggianti! I topi trattati con NO2-OA hanno mostrato un netto miglioramento della funzione diastolica. Parametri chiave come il rapporto E/e’ (un indice di pressione di riempimento del ventricolo sinistro) e il tempo di rilassamento isovolumetrico (IVRT) sono tornati quasi alla normalità. In pratica, il loro cuore aveva ricominciato a rilassarsi molto meglio tra un battito e l’altro.
Non solo:
- La capacità di esercizio, che era significativamente ridotta nei topi con HFpEF non trattati, è migliorata notevolmente nel gruppo NO2-OA. Potevano correre di più!
- L’area dell’atrio sinistro, che si ingrandisce quando il ventricolo sinistro fa fatica a riempirsi, si è normalizzata nei topi trattati.
- Anche i segni di ipertensione polmonare (come l’ispessimento delle arteriole polmonari) erano ridotti.
È importante notare che l’NO2-OA ha ottenuto questi benefici funzionali senza però modificare significativamente l’ipertrofia cardiaca o la fibrosi interstiziale, né l’infiammazione sistemica generale. Questo suggerisce che il suo meccanismo d’azione sia più mirato alla funzione cellulare e metabolica del cuore. Abbiamo anche verificato che questi effetti positivi si manifestavano sia nei topi maschi che nelle femmine.
Uno Sguardo Dentro le Cellule: La Rivoluzione Mitocondriale
Ma come fa l’NO2-OA a migliorare così tanto la funzione cardiaca? Per capirlo, siamo andati a vedere cosa succedeva a livello molecolare, analizzando il proteoma del tessuto ventricolare sinistro (cioè l’insieme di tutte le proteine presenti). E qui abbiamo avuto una sorpresa!
Mentre i topi con HFpEF non trattati mostravano cambiamenti relativamente modesti nel loro proteoma rispetto ai controlli sani, i topi trattati con NO2-OA presentavano un quadro completamente diverso: oltre un quarto delle proteine identificate era significativamente aumentato! E la cosa più straordinaria? Una grandissima parte di queste proteine “potenziate” erano proteine mitocondriali.
I mitocondri, le nostre centrali energetiche cellulari, sembravano essere al centro dell’azione del NO2-OA. Analisi più approfondite con la microscopia elettronica a trasmissione hanno confermato questo sospetto: i cuori dei topi trattati con NO2-OA avevano un numero significativamente maggiore di mitocondri, anche se di dimensioni leggermente più piccole. Più centrali energetiche, anche se più compatte! Questo combaciava perfettamente con l’aumento delle proteine della membrana mitocondriale esterna che avevamo visto nel proteoma.
Inoltre, il DNA mitocondriale era aumentato, così come un fattore chiave per la sua trascrizione (TFAM), suggerendo un processo attivo di biogenesi mitocondriale (la creazione di nuovi mitocondri).
Il Regista dell’Orchestra: L’Attivazione dell’AMPK
Tutto questo fervore mitocondriale doveva avere un regista. L’analisi bioinformatica dei dati proteomici ha puntato il dito su un percorso di segnalazione cruciale per il metabolismo energetico e la salute mitocondriale: la via dell’AMPK (protein chinasi attivata dall’AMP).
L’AMPK agisce come un sensore energetico della cellula: quando l’energia scarseggia, si attiva e promuove processi che generano ATP, come la combustione dei grassi (FAO), e stimola la biogenesi e il “riciclaggio” (mitofagia) dei mitocondri per mantenerli efficienti. Ebbene, nei cuori dei topi trattati con NO2-OA, abbiamo trovato livelli significativamente più alti di AMPK attivata (fosforilata)!
L’attivazione dell’AMPK porta con sé anche l’aumento di altre molecole importanti come le sirtuine (SIRT1 e SIRT3), proteine che aiutano a regolare il metabolismo e la longevità cellulare, spesso lavorando in sinergia con l’AMPK per ottimizzare la funzione mitocondriale.
Mitocondri Potenziati e Metabolismo Ribilanciato
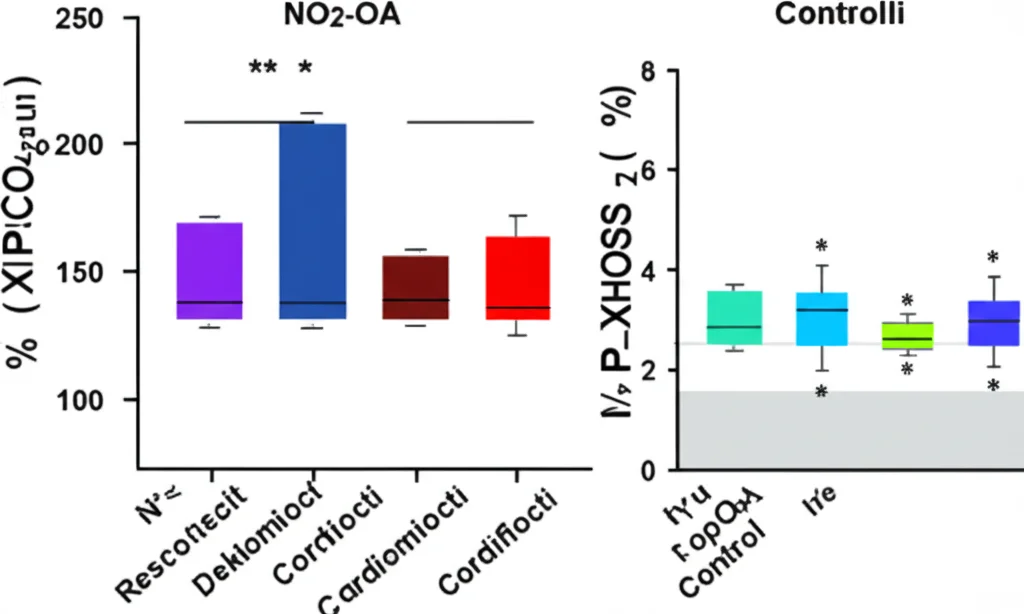
Ma questi mitocondri più numerosi funzionavano anche meglio? Assolutamente sì! Abbiamo isolato i cardiomiociti (le cellule muscolari del cuore) dai diversi gruppi di topi e ne abbiamo misurato la respirazione mitocondriale. I risultati sono stati netti: le cellule dei topi trattati con NO2-OA mostravano una capacità significativamente maggiore di produrre energia sia utilizzando acidi grassi (tramite l’enzima CPT1B) sia utilizzando altri substrati (OXPHOS). Le loro centrali energetiche erano più potenti!
Questo aumento della capacità di bruciare grassi era coerente con l’aumento, visto nel proteoma, di proteine coinvolte nel metabolismo lipidico, come la stessa CPT1B e il trasportatore di acidi grassi FAT/CD36. Sembrava che l’NO2-OA stesse aiutando il cuore a gestire meglio l’eccesso di grassi, utilizzandoli in modo più efficiente per produrre energia invece di accumularli in forme potenzialmente tossiche. Infatti, osservando le goccioline lipidiche all’interno dei cardiomiociti isolati, abbiamo notato che erano significativamente ridotte nei topi trattati con NO2-OA rispetto ai topi HFpEF non trattati.
Inoltre, l’NO2-OA ha migliorato anche il metabolismo del glucosio. I topi trattati mostravano una migliore tolleranza al glucosio e una riduzione del peso corporeo. A livello cardiaco, abbiamo visto una tendenza alla normalizzazione dei livelli di proteine chiave per l’utilizzo del glucosio, come il trasportatore GLUT4 (che era diminuito nell’HFpEF) e l’enzima PDK4 (che era aumentato, bloccando l’uso del glucosio).
Implicazioni e Prospettive Future
Quindi, mettendo insieme tutti i pezzi: l’acido nitro-oleico sembra migliorare la funzione diastolica e ridurre i sintomi dello scompenso cardiaco HFpEF agendo profondamente sul metabolismo energetico del cuore. Lo fa potenziando numero e funzione dei mitocondri, probabilmente attraverso l’attivazione della via di segnalazione dell’AMPK. Questo permette al cuore di gestire meglio sia i grassi che gli zuccheri, producendo più energia e riducendo l’accumulo di lipidi potenzialmente dannosi. Un cuore con più energia e meno “stress” metabolico è un cuore che può rilassarsi meglio.
Certo, questo è uno studio preclinico su topi, e ci sono ancora aspetti da approfondire (come misurare direttamente i livelli energetici nel cuore o studiare modelli più anziani). Tuttavia, i risultati sono estremamente promettenti. Il fatto che l’NO2-OA sia già in fase di sperimentazione clinica sull’uomo (un trial di Fase II è in corso su pazienti obesi con asma) per valutarne sicurezza ed effetti metabolici e infiammatori, rende queste scoperte ancora più rilevanti.
Considerando la crescente prevalenza dell’HFpEF e la mancanza di terapie mirate, l’acido nitro-oleico, con il suo meccanismo d’azione unico focalizzato sul miglioramento della funzione mitocondriale e del metabolismo cardiaco, potrebbe davvero rappresentare una nuova, importante freccia al nostro arco terapeutico. Una piccola molecola con un potenziale enorme per aiutare tanti cuori affaticati!
Fonte: Springer







